Pharma Focus
CDK4/6 억제기전 최초의 유방암 1차 치료제, '입랜스'
화이자, 세계 시장 입지 선점으로 종양 치료 분야 강자로 부상할 가능성 높혀
- 김윤미 기자 kym@medifonews.com
- 등록 2017-01-18 15:08:59
최근 한국은 미국, 서유럽, 일본, 호주 등 고소득 국가들과 함께 암 발생률이 가장 높은 국가들 중 하나로 분류된다. 그중 유방암 발생률의 경우 한국인은 10만 명당 52.1명으로 아시아권 중 일본의 51.5명 대비 높은 발생률을 보이고 있다.
한국의 유방암 5년 상대생존율은 2008년~2012년 기준 91.3%로 지속적 증가 추세를 보이고 있고, 미국의 89.2%, 일본의 89.1% 등 주요 의료 선진국에 비해 앞선 수준이지만, 미국을 비롯한 서양 국가에서는 60~70세 연령층에서 유방암이 가장 많이 발병하는 반면 국내 유방암 진단 평균 연령값은 2012년 기준 51세로 서양 국가 대비 좀 더 이른 나이에 유방암을 진단받는 것으로 알려져 있다.
일반적으로 유방암은 발병연령이 어릴수록 종양이 크고 공격적인 경향이 강하며, 전이 가능성이 높다고 알려져 있어, 상대적으로 유방암 진단 연령이 낮은 한국인에서 좀 더 높은 위험성을 보인다고 유추할 수 있다.
한편, 전이성 유방암(Metastatic Breast Cancer; mBC)은 가장 진전된 단계(4기)의 유방암으로 종양이 뇌, 폐, 뼈, 간 등 신체의 다른 부위로 퍼져 전이가 된 경우를 의미하는데, 국내 유방암 환자 중 전이성 유방암으로 최초 진단을 받는 여성은 5% 미만에 불과하지만 유방암 초기 진단 및 조기 치료를 받은 국내 여성의 40%는 전이성 유방암으로 진행됐다고 한다.
유방암 진단을 받고 조기에 치료되더라도, 첫 진단 이후 5년 혹은 10년, 15년 뒤 전이성 유방암으로 이어질 수 있다는 것이다.
전이성 유방암의 치료는 완치를 목표로 하기보다는 암의 진행을 최대한 지연시키고, 적절한 통증 관리 등 고통 완화 치료(palliative care)를 통해 암으로 인한 영향을 최소화하고 환자가 최대한 삶의 질을 유지할 수 있도록 돕는 데 있다.
유방암의 치료는 발생연령, 병기, 암의 병리학적 특성, 환자의 심리상태 등을 고려해 수술, 방사선치료, 항암화학요법, 내분비치료, 표적치료 등 적절한 치료법을 적용하게 된다.
 최근 국내에 이러한 유방암 치료에 새로운 치료기전을 제시하며 출시된 치료제가 있는데, 한국화이자제약의 ‘입랜스(성분명: palbociclib)’가 바로 그 제품이다.
최근 국내에 이러한 유방암 치료에 새로운 치료기전을 제시하며 출시된 치료제가 있는데, 한국화이자제약의 ‘입랜스(성분명: palbociclib)’가 바로 그 제품이다.
입랜스는 진행성 혹은 전이성 HR+/HER2- 유방암 환자에 대한 1차 표준 치료제로서 1) 폐경 후 여성의 1차 내분비요법으로서 레트로졸(letrozole)과 병용, 2) 내분비요법 후 질환이 진행된 여성에서 풀베스트란트(fulvestrant)와 병용한다.
입랜스는 최초의 CDK 4/6 억제 유방암 치료제로서 그 약물기전의 혁신성을 인정 받아 지난 2013년 4월 FDA로부터 혁신적 치료제로 인정됐고, 신속심사를 거쳐 2015년 2월 FDA로부터 제품허가를 획득했다. 이후 2016년 2월 풀베스트란트와의 병용요법 적응증 확대를 거쳐 같은 해 8월 한국에 입성했다.
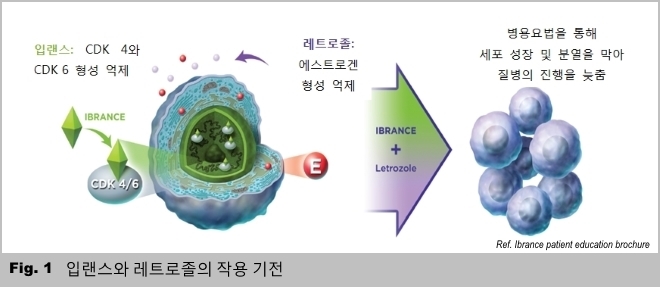
입랜스는 CDK (Cyclin-dependent Kinase) 4/6을 선별적으로 억제하는 경구용 제제로서, 세포주기를 복원하고 암세포의 증식을 막는다. CDK는 세포의 분열과 성장을 조절하는 단백질의 일종이며, CDK 4/6은 세포분열 과정 중 G1 단계에서 S 단계로 진행하는 과정에 관여하는 세포주기 조절 단백질이다.
입랜스와 레트로졸의 병용요법으로 입랜스의 선택적 CDK 4/6 억제기전을 통해 CDK 4/6의 형성을 저해하고, 레트로졸을 통해 에스트로겐 형성을 억제함으로써 암세포의 성장 및 분열을 막아 암세포가 무제한 증식하는 것을 막을 수 있다(Fig. 1).
화이자제약은 폐경 후 HR+/HER2- 진행성 유방암 환자에서의 입랜스/레트로졸 병용요법과 레트로졸 단독요법의 무진행 생존기간(Progression Free Survival: PFS)을 비교 분석하는 PALOMA-1 임상시험(2상)을 진행하였고, 그 결과를 2014년 12월 The Lancet Oncology 온라인을 통해 발표했다.
PALOMA-1 연구는 한국, 미국, 프랑스, 러시아 등 12개 국가 165명 환자를 대상으로 폐경 후 HR+/HER2- 진행성 유방암 환자에 대한 1차 치료제로서 입랜스/레트로졸 병용 투여군(반복되는 4주간의 치료주기 중 3주에 걸쳐 1일 1회 125 mg 투여)과 레트로졸 단독 투여군(2.5 mg을 1일 1회 지속적으로 투여) 간의 무진행 생존기간을 비교, 평가한 무작위 배정, 다기관, 다국적 임상연구이다.
레트로졸과의 병용으로 무진행 생존기간 2배가량 증가
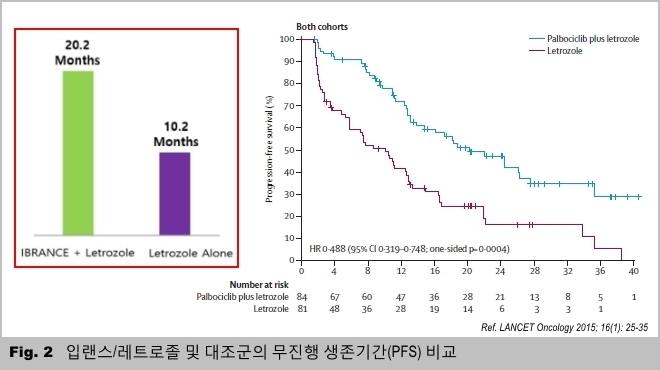
PALOMA-1 임상을 통해 입랜스/레트로졸 병용요법이 레트로졸 단일요법 대비 무진행 생존기간(PFS) 중간값을 2배 가량 연장시킨 것으로 확인됐다.
입랜스/레트로졸 병용 투여군(84명)에서 무진행 생존기간(중간값)이 20.2개월, 레트로졸 단독 투여군(81명)은 10.2개월로 나타나, 병용 투여군에서 무진행 생존기간이 2배 가량 증가했다(Fig. 2).
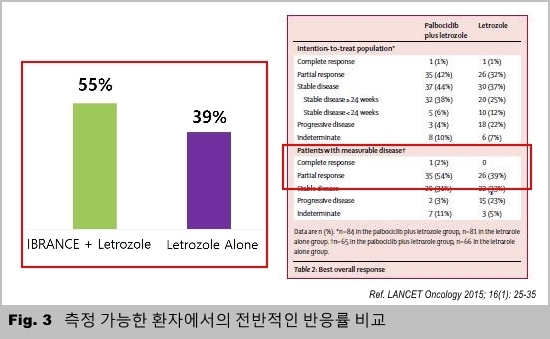
또한 PALOMA-1 임상에서 치료 초기 질병 측정이 가능한 환자 대상으로 종양 축소 등 치료에 따른 반응을 측정하는 객관적 반응률(Objective Response Rate: ORR) 분석 결과, 입랜스/레트로졸 병용군은 ORR 55%로 레트로졸 단독군의 39%에 비해 높게 나타났다(Fig. 3). 입랜스/레트로졸 병용의 종양 축소 효과를 유추할 수 있는 부분이다.
화이자는 이후 폐경 후 HR+/HER2- 진행성 유방암 환자에서의 입랜스/레트로졸 병용 투여군과 레트로졸/위약 투여군 간의 무진행 생존율을 비교, 평가한 PALOMA-2 임상시험(3상)을 통해 PALOMA-1 연구에서의 입랜스/레트로졸 병용의 유의미한 임상적 효과와 안전성 프로파일을 재확인했다. PALOMA-2 임상은 전 세계 17개국 186개 기관을 통해 666명의 환자를 대상으로 진행된 무작위 배정(2:1), 다기관, 다국적, 이중맹검 임상이다.
미국종합암네트워크, 유방암 치료 가이드라인 통해 입랜스/레트로졸 1차 치료제 권고
미국종합암네트워크(National Comprehensive Cancer Network; NCCN)는 최근 2016년 NCCN 침윤성 유방암 치료 가이드라인을 통하여 HR+/HER2- 전이성 유방암 환자에서의 입랜스/레트로졸 병용요법을 1차 치료 옵션 중 하나로 권고했다.
아시아 환자에서의 입랜스/레트로졸 병용 효능∙안전성 프로파일 확인
또한 최근 2016 유럽종양학회 아시아회의(ESMO Asia)에서 발표된 연구 분석 결과로 아시아 환자군에서의 입랜스/레트로졸 병용 효능과 안전성이 비아시아 환자군에서의 결과와 다르지 않음을 확인하며 입랜스의 효능과 안전성 데이타를 추가적으로 확보했다.
이번 발표된 결과는 PALOMA-2 임상의 하위 그룹 연구로 PALOMA-2 임상에 참여한 아시아(95명), 비아시아(571명) 그룹 데이터를 비교 분석했다.
그 결과 아시아 그룹의 입랜스/레트로졸 병용 투여군의 무진행 생존기간(중간값)은 25.7개월을 기록해, 레트로졸 단독 투여군의 13.9개월에 비해 약 11.8개월 개선 효과를 보였다. 비아시아 그룹에서도 입랜스/레트로졸 병용 투여군은 24.8개월, 레트로졸 단독 투여군은 15.9개월을 나타내 약 8.9개월 연장 효과가 나타났다.
종양 축소 등 치료에 따른 질병 반응을 측정하는 객관적 반응률(ORR)과 임상으로 인한 완전관해, 부분관해, 안정병변 달성 여부를 측정하는 임상효용율(CBR)은 측정 가능한 질병군에서 아시아, 비아시아 그룹 모두 레트로졸 단독 투여군 대비 유사한 개선 효과를 보였다.
아시아 그룹의 입랜스/레트로졸 병용군은 ORR 62%, CBR 85%를 보였으며, 레트로졸 단독투여군은 ORR 56%, CBR 74%를 기록했다. 비아시아 그룹의 입랜스/레트로졸 병용군은 ORR 61%, CBR 86%을 기록했고, 레트로졸 단독투여군은 ORR 48%, CBR 72%로 나타났다.
한편, PALOMA-2의 안전성 데이터는 PALOMA-1과 일관되게 나타나고 있으며 예상하지 못한 안전성 이슈는 관찰되지 않았다. 아시아와 비아시아 그룹 비교 시에도 대부분 결과는 일치했다.
백혈구감소증이 가장 흔한 이상반응으로 나타났으나 지지요법 혹은 용량조절을 통해 관리 가능한 수준이었으며, 이상반응으로 인한 치료중단은 아시아 그룹과 비아시아 그룹 각각 10.8%, 9.5%로 비슷했다. 또한 아시아 그룹에서 호중구감소성 발열 사례는 발견되지 않았다.
화이자, 입랜스 선전으로 종양 치료제 시장 강자로 급부상 가능성 높혀…
한편, 지난 11월 화이자는 입랜스의 EU 승인을 발표하며, 입랜스가 유럽시장에 진출한 최초의 CDK4/6 억제 유방암 치료제가 됐음을 선포했다.
유럽 또한 유방암은 여성에서 발병하는 가장 흔한 침윤성 암으로, 매년 464,200명이 새롭게 유방암 진단을 받으며, 131,260명이 유방암으로 사망하고 있다. 또한 초기에 유방암 진단과 치료를 받은 여성의 30% 이상이 전이성 유방암으로 진행하는 것으로 알려져, 새로운 치료기전의 입랜스 출시가 유럽의 유방암 환자들에게 새로운 치료옵션이 될 것이라 기대를 모으고 있다.
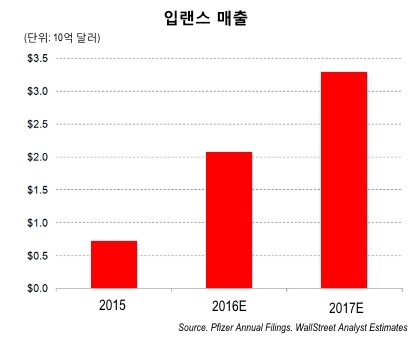 월스트리스 애널리스트들의 전망에 따른 입랜스의 판매 예측은 2016년 21억 달러, 2017년 33억 달러까지 이르고 있다.
월스트리스 애널리스트들의 전망에 따른 입랜스의 판매 예측은 2016년 21억 달러, 2017년 33억 달러까지 이르고 있다.
입랜스가 이미 8,500명의 의료진에 의해 4만 명 이상의 환자들에게 처방되었으며, 이를 근거로 입랜스의 강력한 효능과 안정성 프로파일을 갖춰나가고 있고, 이미 유럽에서도 승인된 점, 그리고 화이자 측이 유방암 외에 편평상피세포와 경부암, 외투세포림프종, 췌장암 등에서의 입랜스의 다각적인 쓰임을 모색 중인 점을 들어 입랜스의 성공이 화이자를 종양 치료제 분야에서 릴리, 머크, BMS와 함께 경쟁할 강력한 위치에 올려놓을 것이라 예측하고 있다.
한편 비슷한 기전의 CDK 4/6 억제 유방암 치료제인 노바티스의 ‘리보시클립(Ribociclib)이 최근 FDA의 우선심사 승인을 받으며, FDA와 EMA에 동시에 허가신청이 접수된 상태로 입랜스의 뒤를 바짝 추격하고 있다.
이에 미국과 유럽, 아시아 등지에서 입랜스가 CDK 4/6 억제제로서 종양 치료제 시장에 우선적으로 입지를 굳혀 판매 고공행진을 계속 이어나갈 수 있을지 향후 귀추가 주목되는 부분이다.
- [동정]암젠, 아동·청소년 생명과학 교육 캠페인 서울시장 표창 수상
- [동정]칠곡경북대병원 성인 수두증 클리닉, 30억원 치매극복 기술개발 과제 수주
- [동정]갑상선 수술 관련 비디오 후두경 통한 기관삽관 유용성 입증
- [동정]한국머크 바이오파마, ‘일∙가정 양립 우수 기업’ 선정
- [동정]고대 구로병원 송준영 교수, 질병청·국립보건연구원 학술연구용역 과제 선정
- [동정]일동후디스 하이뮨, 브랜드파워 단백질보충제 부문 2년 연속 1위
- [동정]서울성모병원 정미향 교수, 국제학술지 유럽예방심장학회지 부편집장 임명
- [동정]한올바이오파마, 국가산업대상 ‘연구개발’ 부문 수상
- [동정]제주대병원 연구팀, 국제학술지에 심장재활 논문 게재
- [동정]동화약품, 박진 신임 공장장 취임















