다케다, 궤양성대장염∙크론병 치료제 ‘킨텔레스’ 등판
장에만 작용하는 항-인테그린 제제로 타 약제 비해 전신 부작용 적어
- 김윤미 기자 kym@medifonews.com
- 등록 2017-08-18 05:40:00
 한국다케다제약(대표 마헨더 나야크)은 지난 17일 ‘궤양성 대장염 ∙ 크론병 치료제 ‘킨텔레스’ 기자간담회’를 개최하고 킨텔레스의 급여 출시 소식을 알렸다.
한국다케다제약(대표 마헨더 나야크)은 지난 17일 ‘궤양성 대장염 ∙ 크론병 치료제 ‘킨텔레스’ 기자간담회’를 개최하고 킨텔레스의 급여 출시 소식을 알렸다.
‘킨텔레스’는 중등도에서 중증의 성인 활성 궤양성 대장염 및 크론병 치료제로, TNF-α 억제제 치료에 실패한 환자를 대상으로 지난 1일 보험급여 적용을 받았으며, 킨텔레스 치료 이후에도 이전에 사용하지 않은 TNF-α 억제제로 교체투여 시 급여가 인정된다.
‘킨텔레스’는 궤양성 대장염과 크론병 치료의 첫 번째 항-인테그린 제제로 기존 약제들과는 달리 장을 표적으로 하여 작용한다.
염증성 장질환은 면역세포가 계속 장으로 유입되어 장에서 염증이 지속되는 상태로, 면역세포의 유입은 장으로 가는 면역세포 표면의 ‘α4β7’ 인테그린이 장 조직에 주로 있는 ‘MAdCAM-1’과 결합하면서 일어난다.
‘킨텔레스’는 면역세포 표면의 ‘α4β7’ 인테그린에 결합해 염증세포가 장 조직으로 유입하는 것을 차단함으로써 치료효과를 나타낸다.
즉, ‘킨텔레스’는 기존 타 약제들과는 달리 장에서만 선택적으로 작용하여 전신적인 부작용이 적고, 추가적인 염증세포의 유입으로 인한 장기적인 염증을 차단한다.
회사 측에 따르면, ‘킨텔레스’는 현재까지 6건의 임상시험을 통해 2,830명의 환자에게서 우수한 안전성 프로파일을 입증했다.
그중 최근 발표된 궤양성대장염 환자에서 TNF-α 억제제 경험이 없는 환자와 TNF-α 억제제에 실패한 환자에 대한 ‘킨텔레스’ 효과를 각각 분석한 GEMINI-I 임상의 사후비교분석(post-hoc analysis) 연구 따르면, ‘킨텔레스’가 TNF-α 억제제 경험 여부와 상관없이 6주차 임상적 반응(clinical response)을 보인 환자에서 52주에 임상적 관해(clinical remission)를 유도했음을 알 수 있다.
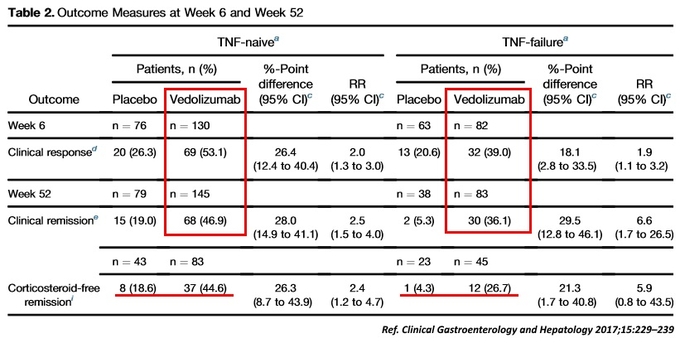
또한 ‘킨텔레스’의 GEMINI LTS 연구를 통한 장기 효과를 분석한 결과, 킨텔레스에 유도기간(induction phase) 동안 반응을 보인 환자 중 약 80~90%가 152주까지 임상적 관해가 유지됐다(연구 중단 또는 152주 미도달 환자 데이터를 치료 실패로 간주할 경우는 35~50%).
궤양성 대장염과 크론병은 증상의 악화와 재발을 반복하며 완치가 되지 않는 만성염증성장질환 중 하나다. 그동안 궤양성 대장염 및 크론병 치료에는 다양한 치료제들이 있음에도 불구하고 기존 치료제에 대한 충족되지 않은 요구가 여전히 존재해 왔다.
‘킨텔레스’ 허가 이전까지 유일한 생물학적 치료 옵션이었던 TNF-α 억제제의 경우, 해당 치료를 받은 환자의 최대 40%가 초기에 반응이 없는 것으로 나타났다. 치료 시작 1년 후 TNF-α 억제제에 반응을 소실하는 환자도 20~40%나 된다. 또한, TNF-α 억제제는 전신작용으로 인한 감염의 위험 증가 가능성이 있다.
 이번 출시 기자간담회에 연자로 참석한 고려의대 소화기내과 진윤태 교수는 “궤양성 대장염, 크론병은 만성 질환으로 평생 관리가 필요하므로, 오랫동안 관해를 유지할 수 있고 안전성 프로파일이 확인된 치료제가 필요하다. 스테로이드로 안 듣는 환자에게 쓸 수 있는 약제가 지금까지 매우 제한적이었다”며, “효과와 안전성 프로파일 측면 모두에서 킨텔레스가 TNF-α 억제제 치료에 실패한 환자들에게 새로운 치료 옵션으로 분명한 이점을 제공할 것으로 보인다”고 설명했다.
이번 출시 기자간담회에 연자로 참석한 고려의대 소화기내과 진윤태 교수는 “궤양성 대장염, 크론병은 만성 질환으로 평생 관리가 필요하므로, 오랫동안 관해를 유지할 수 있고 안전성 프로파일이 확인된 치료제가 필요하다. 스테로이드로 안 듣는 환자에게 쓸 수 있는 약제가 지금까지 매우 제한적이었다”며, “효과와 안전성 프로파일 측면 모두에서 킨텔레스가 TNF-α 억제제 치료에 실패한 환자들에게 새로운 치료 옵션으로 분명한 이점을 제공할 것으로 보인다”고 설명했다.
하지만 이번 급여 대상이 ‘TNF-α 억제제 치료에 실패한 환자’로 제한되어 있어 추후 확대 필요성이 남아 있는 상태다.
‘킨텔레스’는 이미 2014년 미국과 유럽에서 승인되었으며, 그 대상 또한 ‘코르티코스테로이드’나 ‘면역조절제’, ‘종양괴사인자(TNF) 차단제’ 등 한 가지 이상의 표준요법제들로 충분한 반응을 이끌어 내지 못한 환자들로, 국내의 급여 적용 범위가 협소한 편이다.
회사 측은 이에 대해 “이미 선진국들에서 한국보다 광범위한 적응증으로 허가 받아 사용되고 있는 만큼 효과와 안전성이 입증된 상황으로, 국내에서의 적응증 확대도 지속적으로 추진할 것”이라고 전했다.
다케다가 공시한 2016년도 연간보고서에 따르면, ‘킨텔레스(글로벌상품명 엔티비오)’는 2014년 6월 출시 이후 매출이 급성장하며 2016년까지 누적 10억 달러(약 1조 1,354억 원)의 매출을 달성했다. ‘킨텔레스’의 매출 성장에 힘입어 다케다의 위장관질환 분야 매출이 전년 대비 23.6% 상승한 것으로 나타났다.
다케다는 ‘킨텔레스’를 향후 매출성장을 견인할 주요 품목으로 꼽고 있으며, 오는 2018년 말까지 ‘킨텔레스’의 연매출 20억 달러(2조 2,746억 원) 달성을 목표로 잡고 있는 만큼 글로벌 시장에서도 국내 시장에서도 공격적인 마케팅을 펼칠 것으로 예상되고 있다.
- [동정]암젠, 아동·청소년 생명과학 교육 캠페인 서울시장 표창 수상
- [동정]칠곡경북대병원 성인 수두증 클리닉, 30억원 치매극복 기술개발 과제 수주
- [동정]갑상선 수술 관련 비디오 후두경 통한 기관삽관 유용성 입증
- [동정]한국머크 바이오파마, ‘일∙가정 양립 우수 기업’ 선정
- [동정]고대 구로병원 송준영 교수, 질병청·국립보건연구원 학술연구용역 과제 선정
- [동정]일동후디스 하이뮨, 브랜드파워 단백질보충제 부문 2년 연속 1위
- [동정]서울성모병원 정미향 교수, 국제학술지 유럽예방심장학회지 부편집장 임명
- [동정]한올바이오파마, 국가산업대상 ‘연구개발’ 부문 수상
- [동정]제주대병원 연구팀, 국제학술지에 심장재활 논문 게재
- [동정]동화약품, 박진 신임 공장장 취임















