올 해 1/4분기 보고내용, 부작용 확인 위해 심사중인 정보
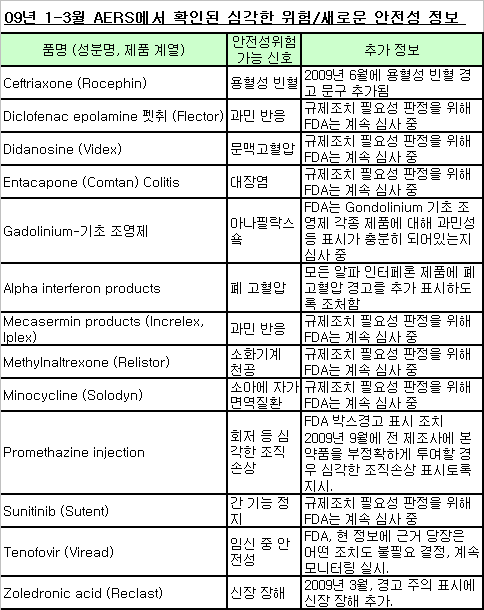
미국 FDA는 2009년 1-3월까지 부작용 보고시스템 AERS(Adverse Event Reporting System)에서 확인된 로세핀 등 13개 약품들의 부작용 가능성을 심사중인 안전성 정보를 예고했다.
FDA는 이번 발표내용이 부작용 발생 가능성을 확인했다는 의미이지, 약물과 발표된 위험성과의 관계를 확인했다는 뜻은 아니라고 분명히 밝혔다.
FDA는 앞으로 더 평가해서 약물이 위험성과 관련이 있다고 판단되면 표시 변경을 포함한 각종 조치를 취할 수 있다고 설명했다.
즉 위험평가 해소전략(REMS)이나 약물의 위험성에 대한 보다 구체적인 추가 자료 수집 등이 요청된 후 평가하고 적절한 조치를 취하겠다는 것.
따라서 FDA는 다음 표에 제시된 약물에 대해 처방하지 말라는 의미가 아니며 또한 투약을 중단하라는 의미가 아님을 강조하고 있다.
김윤영 기자 yunyoung,kim@medifonews.com
< 저작권자 © Medifonews , 무단전재 및 재배포금지 >
- 본 기사내용의 모든 저작권은 메디포뉴스에 있습니다.
