[내분비대사내과] 이상지질혈증 가이드라인, 무엇이 달라졌나?
윤지성(영남대학교병원 내분비대사내과)
- 윤지성 medifonews@medifonews.com
- 등록 2021-03-26 10:53:51

심혈관질환은 전 세계적으로 가장 많은 사망 원인으로, 국내 역학조사에 의하면 관상동맥질환은 증가하는 반면 뇌혈관질환 발생은 감소하고 있는데, 그 중에서도 뇌출혈 유병률은 빠르게 감소하고 있으나, 뇌경색의 발생은
오히려 증가되고 있다. 이는 죽상동맥경화증 유발의 직접적인 원인인 이상지혈증의 증가가 주된 원인의 하나로
추정되며, 실제 이상지혈증의 유병율은 전 세계적으로 증가하고 있다. 국내 이상지혈증의 유병률은
2014~2016년 통계자료에 의하면 한국30세 이상 성인
기준으로 40% 정도로 보고되고 있다.
2013년 AHA/ACC(미국심장학회) 가이드라인에서는 기존의 “treat to target”이라는 패러다임에서 과감하게 벗어나 스타틴 치료가 필요한 네 그룹을 정의하면서, 스타틴 자체의 치료에 포커스를 맞추고, LDL-C 목표는 절대치보다는
기저치에서의 상대적 감소를 강조하였다. 이후 추가적인 대규모 임상연구에서 비스타틴제의 효과와 LDL-C 목표치에 대한 결과들이 발표됨에 따라 이를 포함한 개정안이 2018년
발표되었다.
한국지질동맥경화학회는
국내외 연구결과와 해외의 최신 치료지침을 참고하여 좀더 세분화된 치료 기준을 정하고, 새로운 약물들의 치료 전략 등을 포함한 제4판 이상지질혈증 진료지침을 2018년 발표하였다. 따라서 이와 같은 최신 진료지침의 주된 변화를
살펴보았다.
이상지혈증의 진단
미국심장학회에서는 혈중 지질 측정에 대해 몇 가지 변화를 보였는데, 첫번째로는 비공복상태에서의
지질측정이다. 공복 측정은 환자 및 의사 모두에게 불편함을 안겨줄 뿐 아니라 위험도 평가에 추가적인
이점을 주지 못하므로, 일반적으로 약물 치료 전 스크리닝 등의 목적으로 시행하는 경우 공복 여부에 관계없이
측정하도록 하였다. 하지만
비공복 측정결과 중성지방이 400 mg/dL이상인 경우 공복상태에서 재측정하도록 하였다. 또한 LDL-C이 70 mg/dL미만인
경우에는 LDL-C을 직접 측정하거나 이전의 Freidewald 공식이
아닌 변형된 LDL 공식을 사용할 것을 권유하였다. 이는
Martin/Hopkins LDL-C측정법으로 기존 Freidewald
공식이 중성지방값을 5로 나누어 계산하는 대신, 각
환자의 중성지방 값과 non-HDL-C 값에 근거한 TG:VLDL
ratio를 적용하여 계산하는 것으로, 직접측정법에 더 근접한 값을 보여준다.

반면, 지질강하제의 치료시작이나 용량조절 후 4~12주, 그리고 매 2~12개월마다 공복 지질혈당 검사를 시행하여 약제의
치료 효과와 순응도 등을 모니터링하도록 하였다.
한국지질동맥경화학회에서는
기존의 Friedewald 공식을 이용한 LDL-C의 간접측정은
직접측정값보다 낮게 나와 심혈관질환의 발생 위험도가 저평가될 수 있으므로 중성지방 농도와 무관하게 LDL-C 직접측정법으로
하여 한계점을 극복할 수 있음을 강조하였다
위험도 분류 및 치료기준
미국심장학회의 새로운 가이드라인에서 눈에 띄는 변화 중의 하나는 비스타틴 치료제의 병용요법으로, 추가된 대규모 무작위배정 임상연구
결과들에 근거하여 비스타틴계열의 지질강하제(ezetimibe, proprotein convertase
subtilisin/kexin type 9 (PCSK9) 억제제 (alirocumab or
evolocumab))를 선택적으로 병용할 수 있도록 하였다. ezetimibe의 병용치료를 뒷받침하는 연구는 2015년 발표된 IMPROVE-IT으로, 10일 이내의 급성관상동맥증후군 환자 18,144명을 대상으로 simvastatin 단독보다 ezetimibe를 병용투여한 군에서
7년내 심혈관질환 발생이 감소되었다(HR, 0.936; P=0.016).
PCSK9 억제제의 병용 투여의 근거가 되는 대표적인 연구로는 2017년 FOURIER와 2018년 ODYSSEY
연구가 있다. FOURIER 연구는 고강도 스타틴 치료에도 LDL–C≥70 mg/dL인
27,564명의 ASCVD 환자에서 평균 2.2년간 evolocumab을 병용투여한 결과 LDL-C를 60%가량 낮추면서 복합성 심혈관질환의 발생을 15% 유의하게 감소시켰다. 병용약제 선택에 중요한 것은 예측되는 LDL-C 감소 정도로, 치료법에 상관없이 LDL-C이 40
mg/dL 감소하면 ASCVD 위험이 약 20~25 % 상대적
감소된다. 고강도 스타틴은 LDL-C을 약 50% 감소시키는 반면, ezetimibe는 추가적으로 20~25% 더 감소시키고, PCSK9 억제제인 evolocumab과 alirocumab은 FDA 승인 용량에서 LDL-C을 약 60% 감소시킨다. 하지만 약제의 추가전에 반드시 환자가 최대용량의 약물복용을 잘하고 있는지, 생활습관
개선을 잘 하고 있는지, 검사가 정확한지 확인해야 한다.
미국심장학회에서는 스타틴 치료 측면에서는 이전처럼 스타틴 치료가 필요한 네 그룹을 유지하면서 일부 요소들을
추가하였다.
1) 죽상동맥경화증성 혈관질환(ASCVD)이 있는
그룹으로, 개정안에서는 급성 관상동맥 증후군, 심근경색, 협심증, 관상동맥 또는 동맥 혈관재건술, 뇌경색, 일과성 허혈, 말초혈관질환, 대동맥류로 정의하고, 고강도의 스타틴을 투여하도록 하였다. 또한 추가 검사 없이 임상적으로 평가하여 초고위험군과 안정성 ASCVD군으로
나누었다.
최근 12개월내 급성 관상동맥 증후군, 심근경색, 허혈성 뇌졸중, ABI<0.85이면서 파행을 동반한 말초혈관질환을
주요 ASCVD로 정의하고, 65세 이상, 가족형 고콜레스테롤혈증, 관상동맥 우회술이나 스텐트시술, 당뇨병, 고혈압, 만성신질환(eGFR 15~59 mL/min/1.73m2), 현재 흡연,
최대용량의 치료에도 지속적으로 LDL-C≥100
mg/dL, 울혈성심부전을 고위험인자로 정의하였다. 이 중 주요 ASCVD 발생이 다발성이거나, 1개의 주요 ASCVD가 있으면서 여러 개의 고위험인자를 동반한 경우를 초고위험군으로 분류하였다.
안정성 ASCVD 그룹은 이전과 같은 권고사항을 적용하여 가능한
최대용량의 스타틴을 사용하고, 그럼에도 불구하고 LDL-C ≥70 mg/dL으로 지속되는 경우 ezetimibe를 추가 병용투여를
권고하였다.
초고위험 ASCVD군에서는
가능한 최대용량의 스타틴 투여에도 LDL-C이 지속적으로 70
mg/dL이상인 경우 ezetimibe를 추가하고, 2제요법에도
여전히 LDL-C이 지속적으로 70 mg/dL이상인 경우, PCSK9억제제를 추가하여 치료함으로써 심혈관질환을 개선시키도록 하였다.
2) 심한 일차성 고콜레스테롤혈증(LDL-C ≥190 mg/dL) 그룹은 ASCVD위험도 평가없이 고강도 스타틴을
투여하고, LDL-C이 지속적으로 100 mg/dL이상인
경우, 특히 조기 ASCVD가족력이 동반된 경우 ezetimibe를 추가하도록 하였다. PCSK9 억제제는 비용-효율성을
따져보고 일부 환자에서 선택될 수 있다.
3) LDL-C≥70 mg/dL인 40~75세의 당뇨병환자에서는 10년
ASCVD 위험도의 측정없이 중강도 스타틴을 바로 투여하도록 변경되었고, 다수의 ASCVD 위험인자를 동반한 경우 고강도 스타틴을 투여하도록 하였다. 특히 10년 ASCVD위험이 20% 이상인
경우, 고강도 스타틴 치료에도 LDL-C이 50% 이상 감소되지 않으면 ezetimibe를 추가 투여하도록 하였다.
4) 40세 이상의 LDL-C≥70<190 mg/dL인 경우로, 2013년 가이드라인에서는 10년 내 ASCVD 발생위험이 ≥7.5%인
경우 스타틴을 바로 투여하도록 권장하면서 과잉치료의 위험이 많았던 반면, 개정안에서는 20% 이상인 경우 고강도 스타틴을 투여하고, 5~20% 사이의 중등도
위험군에서는 위험증강인자(조기ASCVD 가족력, 만성염증성질환, 임신전자간증이나 조기 폐경, 대사증후군, 만성신질환, 지속적으로 LDL-C≥160 mg/dL, 중성지방≥175mg/dL 등)를 고려하여 좀더 세밀한 조정을 하도록 하였다. 10년 위험도가 5.0~7.5%인 경계성 ASCVD 위험 환자에서 위험증강인자가 있으면 class IIb의 권장사항으로 스타틴 치료를 권장하고 7.5~20.0%의
중등도 위험을 지닌 환자에서는 class I의 권장사항으로 스타틴 치료를 권장한다. 이것으로도 확실치 않은 경우 CT촬영을 통한 관상동맥석회화지수(CAC score)가 스타틴 투여 여부 결정에 이용될 수 있다고 하였다. 즉, 10년 ASCVD 위험도가 7.5~20%인
중등도 위험군에서 CAC score가 0인 경우 스타틴 투여를
고려하지 않아도 되는 반면, CAC score가 100이상인
경우 스타틴 투여가 도움이 될 수 있다고 하였다. CAC score가
1~100인 경우에는 의사-환자가 함께 위험도와 이점을 고려하여 스타틴 투여를 결정하도록
하였다. 만약 스타틴을 투여하지 않는 경우 2년후 CAC score를 재측정하도록 하였다.
이처럼 각 그룹에 따라 기저 LDL-C를 50%이상 낮추는 고강도 스타틴 혹은 30~50% 낮추는 중강도 스타틴을
투여하도록 권고하였는데, 이는 스타틴 자체의 다양한 작용효과를 인정하면서, 진료실에서 쉽게 환자를 분류하고 약제를 투여할 수 있도록 한다는 면에서는 장점이 있지만 인종에 대한 고려가
되지 않아 우리나라를 포함한 아시아인에서는 고강도의 스타틴을 장기적으로 투여하는 경우 더 빈번한 부작용의 발생과 과잉치료가 조장될 수 있다는 우려가
잔재한다.
한국지질동맥경화학회에서는 기존 국내의 치료지침과 같이 심혈관질환 위험요인들의 유무에 따라 목표 LDL-C 농도를 설정하는 틀을 유지하되, 구체적인 위험요인들이나 치료 기준에 관해서는 수정보완하였다 (Table 1). 심혈관질환
발생 위험도에 따라 초고위험군, 고위험군, 중등도위험군, 저위험군으로 분류하였는데, 초고위험군은 기존에 심혈관질환이 있는 환자(관상동맥질환, 말초동맥질환, 죽상동맥경화성 뇌졸중 및 일과성 뇌허혈)를 포함하고, 고위험군은 경동맥질환(유의한
경동맥 협착)이나 복부동맥류, 당뇨병이 있는 환자를 포함한다. 경동맥질환의 경우 이전 지침에서는 50%가 넘는 경동맥 협착이 확인된
경우에만 고위험군으로 정의하였으나, 실제 협착의 정도뿐 아니라 경동맥 경화반의 성상도 중요하므로 개정안에서는
심혈관질환의 발생이 예측되는 유의한 경동맥질환으로 수정하였다. 당뇨병 역시 이전부터 고위험군에 속해 있었지만,
단백뇨와 같은 당뇨병성 합병증이 동반되거나 흡연, 고혈압,
조기 심혈관질환의 가족력 등 위험인자가 동반된 당뇨병 환자에 대해 위험도를 더 높게 상향 조정했다.
LDL-C를 제외한 주요 위험인자가 2개 이상인 경우
중등도위험군으로 분류되며, 주요 위험인자가 1개 이하인 경우
저위험군으로 분류된다. 최근 미국임상내분비학회 가이드라인에서는
LDL-C 목표치를 55 mg/dL 미만으로 낮추는 극초고위험군에 대한 권고가 있으나, 국내 권고 사항에는 포함시키지 않았다.
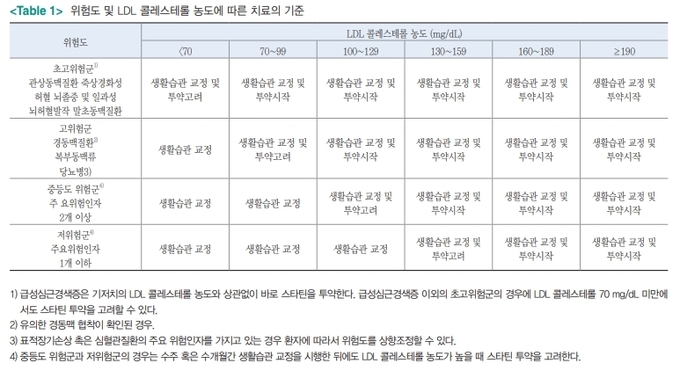
초고위험군의 경우 이차예방을 위해 LDL-C이 70mg/dl 미만이더라도 LDL-C 농도와 무관하게 바로 스타틴을 투여하고 LDL-C이 목표에
도달되지 않을 경우 ezetimibe나 PCSK9 억제제의
병용요법을 권고한다. 스타틴 치료에도 LDL-C 목표치에 도달하지 못할 경우에는 ezetimibe나 PCSK9억제제와의 병용치료를, 스타틴 치료 후 이상 반응이 발생할 경우에는 ezetimibe나 PCSK9억제제 등의 새로운 치료제를 사용하도록
권고했다. 이 외에도 고중성지방혈증 치료 시 니코틴산의 투여에 대한 권고가 삭제되고, 피브린산 유도체와 오메가-3에 대해서만 언급했다. 즉, 중성지방이 500 mg/dL
이상인 경우 급성췌장염의 위험이 증가하므로 이차적인 원인이 없거나 교정된 뒤에도 지속될 경우 피브린산유도체, 오메가 3 등의 약물치료를 시작하고, 중성지방이 200~499 mg/dL 인 경우 스타틴 투여에도 지속적으로
200 mg/dL 이상 지속될 때 위의 약제를 추가 투약하도록 권고하였다.
결론
2018 년 개정된 미국심장학회의
콜레스테롤 가이드라인은 ASCVD 위험을 감소시키기 위해 2013 가이드라인에서
제안된 기본 원칙을 토대로 최근의 대규모 임상결과의 핵심사항을 추가하여, 보다 정확한 LDL-C 산정과 함께 치료의 목표치를 추가하고, 최대한의 스타틴 치료와
함께, ezetimibe, PCSK9 억제제의 병용투여에 대한 가이드라인을 제시하였다. 또한 중등도 위험을 지닌 환자에서 일차예방을 위한 치료결정에 위험증강인자와 관상동맥석회화지수를 활용하도록 함으로써, 좀더 세밀하고 개별화된 예방 치료가 가능할 것으로 기대된다. 하지만
한국인을 대상으로 한 ASCVD발생 위험도를 예측하는 척도가 아직 없어 위험군의 분류에 일부 제한이
존재하며, 보조적인 진단법으로서의 관상동맥석회화지수의 국내 적용에 대한 연구가 필요할 것으로 생각된다.
Reference
1. Stone NJ, Robinson JG, Lichtenstein AH, et
al. 2013 ACC/AHA guideline on the treatment of blood cholesterol to reduce
atherosclerotic cardiovascular risk in adults: a report of the American College
of Cardiology/American Heart Association Task Force on Practice Guidelines. J
Am Coll Cardiol 2014;63:2889-934.
2. Grundy SM, Stone NJ, Bailey AL, et al. 2018
AHA/ACC/AACVPR/AAPA/ABC/ACPM /ADA/AGS/APhA/ASPC/NLA/PCNA guideline on the
management of blood cholesterol: report of the American College of Cardiology/American
Heart Association Task Force on Clinical Practice Guidelines. J Am Coll Cardiol
2018. 72:e91-e220.
3. Committee of Clinical
Practice Guideline of the Korean Society of Lipid and Atherosclerosis (KSoLA).
Korean Guidelines for the Management of Dyslipidemia 4th ed, 2018
4. Cannon CP, Blazing MA,
Giugliano RP, et al; IMPROVE-IT Investigators. Ezetimibe Added to Statin
Therapy after Acute Coronary Syndromes. N Engl J Med 2015;372:2387-2397
5. Schwartz GG, Steg PG, Szarek M, et al;
ODYSSEY OUTCOMES Committees and Investigators. Alirocumab and Cardiovascular
Outcomes after Acute Coronary Syndrome. N Engl J Med. 2018;379:2097-2107.
6.
Sabatine MS, Giugliano RP, Keech AC, et al.; FOURIER Steering Committee
and Investigators. Evolocumab and Clinical Outcomes in Patients with
Cardiovascular Disease. N Engl J
Med. 2017;376:1713-1722.
출처: 디아트리트 VOL.
19 NO. 2
- [인사]보건복지부 과장급 전보 (9/3)
- [동정]대구가톨릭대병원 박기영 교수, 아시아-오세아니아 재활의학회 학술대회서 특별강연·연구발표
- [화촉]남궁승균 JW중외제약 홍보팀 매니저 (9/21)
- [인사]서울성모병원 직원인사(9/1)
- [동정]콜마비앤에이치, ‘한국ESG경영대상’ 중견기업 대상 수상
- [인사]알보젠코리아, 이욱세 신임 대표이사 취임 (9/1)
- [인사]가톨릭대 인천성모병원, 제22대 의무원장에 김종태 교수 선임
- [부음]김강립 前 식품의약품안전처장 모친상
- [인사]경희대학교병원 인사(9/1)
- [인사]가톨릭대 서울성모병원 보직(9/1)
- [동정]대구가톨릭대병원 박기영 교수, 아시아-오세아니아 재활의학회 학술대회서 특별강연·연구발표
- [동정]콜마비앤에이치, ‘한국ESG경영대상’ 중견기업 대상 수상
- [동정]원텍, 탈모치료기 ‘헤어빔’으로 2025 올해의 브랜드 대상 7년연속 수상
- [동정]세노비스, 멀티비타민·키즈 비타민 ‘2025 올해의 브랜드 대상’ 수상
- [동정]충남대학교병원 강민웅 교수, 장영실상 수상
- [동정]원텍, ‘올리지오 키스’로 2025 올해의 브랜드 대상 2년연속 수상
- [동정]휴젤, ‘웰라쥬’ 2025 올해의 브랜드 대상 수상
- [동정]고대 구로병원 이의석 교수, 보건복지부장관 표창 수상
- [동정]GC녹십자, ‘2025 노사문화 우수기업’ 선정
- [동정]길병원 심재앙·이병훈 교수팀, 아시아 정형외과 최고 권위 국제학술대회 ‘최우수 포스터상’ 수상













