[소화기내과] 내시경을 이용한 소화기암의 최신 진단 및 치료
- 문정섭 help@medifonews.com
- 등록 2009-12-28 14:25:56

문 정 섭
인제의대 서울백병원 소화기내과
우리나라 2005년 암 발생분율을 살펴보면 남자는 위암 21.9%, 폐암 15.9%, 간암 14.5%, 대장암 13.2% 순이고 여자는 갑상샘암 16.9%, 유방암 15.1%, 위암 13.5%, 대장암 11.3% 순으로 전반적으로 소화기암의 비율이 높다. 본고에서는 최근에 연구되는 소화기암의 진단과 치료에 대한 소화기내시경 발전을 중심으로 언급하고자 한다. 소화기내시경의 궁극적인 목표는 영상을 개선하여 조직검사 없이 조기에 질환을 진단(optical biopsy)하고 내시경을 이용한 다양한 시술(endoscopic intervention)의 개발이다.
우리나라에서는 1970년 제3차 대한소화기병학회에서 조기위암의 최초 보고가 있었으며 1970년 대한내과학회잡지에 조기위암 종설이 최초로 게재되었다. 조기 소화기암 진단을 위한 최근 발전을 살펴보면 고화질 내시경(high-resolution endoscopy), 확대 내시경(magnification endoscopy), 협대역영상 내시경(narrow-band imaging endoscopy, NBI endoscopy), 다대역영상 내시경(multi-band imaging endoscopy, MBI endoscopy) 등과 같은 내시경 화질을 개선한 내시경과 이전에 관찰이 어려웠던 소장을 관찰하는 캡슐 내시경(capsule endoscopy), 이중 풍선 또는 단일 풍선 소장내시경(double balloon or single balloon enteroscopy) 등이 있다.
내시경을 이용한 시술은 조기위암 치료를 위한 내시경적 점막절제술(endoscopic muc-osal resection, EMR)과 내시경적 점막하박리술(endoscopic submucosal dissection), 내시경초음파(endoscopic ultrasonography)를 이용한 진단 및 치료 이외에도 다양한 여러 시술이 있다.
고화질 내시경
현재 사용하는 내시경은 백색광을 이용하며 영상을 만드는 방법에 따라 크게 적, 녹, 청 3색을 번갈아 비춰주고 돌아오는 영상을 조합하여 최종 영상을 만드는 RGB 연속 비데오스코프(RGB sequential videoscope)와 디지털카메라 같이 자연색을 비춰주고 CCD 소자에 맺히는 영상을 보는 CCD 비데오스코프(CCD videoscope)로 나누어 볼 수 있다. 고화질 내시경은 고화질 CCD를 사용하여 수직 해상도가 1080 line으로 더 선명한 영상을 구현하며 10~71 microns 크기의 물체를 구분할 수 있다.
확대 내시경
확대 내시경은 소화기 점막을 확대 관찰하는 것으로 배율은 1.5~115배이다. 관찰 시에는 미세혈관 구조(microvascular architecture)와 미세표면 구조(microsurface structure)를 같이 관찰하는 것이 포인트이다. 각 장기와 병변에 따른 소견이 모두 다르므로 특징적인 소견을 미리 숙지할 필요가 있다. 정상 식도에서는 혈관이 끝나는 intrapapillary capillary loop(IPCL)가 규칙적으로 잘 보인다. 위장관에서 NBI를 이용한 확대 내시경을 보면 정상 점막은 미세혈관과 점막이 규칙적인데 반해 고도 이형성과 조기암은 미세혈관이 불규칙하고 미세표면은 불규칙하고 병변과 정상 점막 경계가 명확하다.
식도암에서 NBI 확대내시경을 시행하면 기존 내시경보다 식도암의 심달도를 더 정확히 예측할 수 있다. 바렛식도는 초기에 미세혈관과 표면이 규칙적이지만 이형성과 조기암이 동반되면 미세혈관과 표면이 불규칙해 진다. NBI 확대내시경으로 위를 보면 체부와 전정부의 표면 형태가 다르다. 특히 subepithelial capillary network(SECN)과 crypt opening 모양이 다르다. 조기위암에서 확대 내시경의 유용성은 EMR이 가능한 조기 병변을 발견하고 EMR 후 재발을 초기에 진단하는 것이다. 특히 methylene blue 염색 후 확대 내시경은 위 장상피화생과 이형성을 조기에 발견할 수 있다. Kudo는 색소 내시경과 확대 내시경을 이용하여 대장 용종의 pit 패턴의 특징적인 소견을 관찰하여 대장 용종을 비선종형과 선종형/암형으로 구분하였다.
최근에는 modified Kudo 분류가 이용되고 있으며 색소내시경 대신 NBI 확대 내시경을 이용하기도 한다. 색소 내시경은 혈관의 관찰이 어렵지만 NBI는 표면구조 외에 미세혈관 구조까지 관찰이 가능한 장점이 있다.
대비증강 내시경
대비증강 내시경(contrast enhanced endoscopy)은 점막에 색소를 도포하여 진단율을 높이는 색소 내시경을 대신하기 위하여 개발되었다. 이는 색소 내시경과 유사한 영상을 기계적으로 만든다. 영상 구현 방법에 따라 백색광 앞에 협대역 필터를 장착하는 협대역영상 내시경과 소프트웨어를 이용하여 이를 해결한 다대역영상 내시경이 있다. 대비증강 내시경은 대부분 확대 내시경으로 관찰한다. 제한점으로 관찰자 간 차이가 많으며 소견의 구분이 표준화되어 있지 않고 아직 기술적으로 해결해야 할 영상의 문제점이 있다.
1. 협대역영상 내시경
협대역영상 내시경(NBI endoscopy)은 백색 제논 광원 앞에 협대역 필터를 장착하여 적, 녹, 청 3색 중 적색을 제거하고 녹, 청색 파장의 폭을 줄임으로써 선명한 영상을 만든다. 청색은 점막표면, 녹색은 점막심부의 혈관의 선명한 영상을 구현한다. 색소 내시경과 NBI 내시경은 기존 내시경보다 종양 유무를 구분하는데 우수하지만 색소 내시경과 NBI 내시경 간에 차이는 없다. NBI 내시경은 영상이 어둡고 혈액이나 담즙이 있으면 영상이 선명하지 못한 문제점이 있다(Fig. 1).
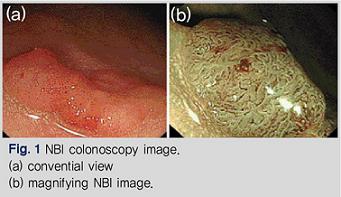
2. 다대역영상 내시경
다대역영상 내시경(MBI endoscopy)은 컴퓨터 소프트웨어를 이용한 가상의 색소내시경으로 여러 가지 세팅의 영상을 만들 수 있다. 방법은 원래의 내시경 영상에서 대역(band)을 좁히고 긴 파장의 빛을 제거하는 것이다.
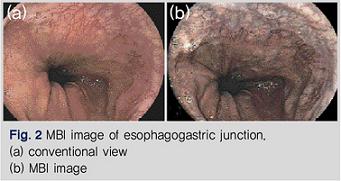
400~580nm 사이 6가지 세팅이 있으며 혈관구조와 점막의 pit 패턴을 잘 볼 수가 있다(Fig. 2). 아직까지 내시경을 빨리 움직일 때 화상이 일그러지는 문제점이 있다. 최근 개발된 SB2 캡슐 내시경에도 MBI 내시경과 유사하게 소프트웨어를 이용한 blue mode 기능이 추가되었다.
직립형 내시경초음파 유도하 세침흡인술
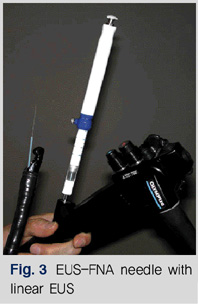
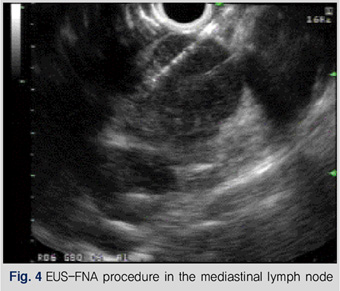
내시경초음파는 주사 방향에 따라 방사형(radial type)과 직립형(linear type)이 있다. 직립형의 장점은 실시간으로 초음파 상을 보면서 조직검사와 시술이 가능하다는 것이다. 직립형 내시경초음파 유도하 세침흡인술(linear EUS-guided fine needle aspiration, EUS-FNA)은 내시경초음파를 이용한 세포검사로서 이 시술이 활성화되면 침습적인 흉강경, 복강경, 시험적 개흉술이나 개복술을 상당히 대체할 수 있다. EUS-FNA는 직립형초음파로 위장관이나 위장관 주위 장기의 병변을 보면서 EUS-FNA 침을 병변에 찌르고 음압을 가한 후 병변 안에서 침의 전후조작을 하여 세포조직을 얻는다(Fig. 3, 4). 국내에서는 입원 후 시행하는 것이 일반적이다. EUS-FNA가 가능한 영역은 식도, 종격동, 위, 좌측부신, 간, 췌장, 담낭, 신장, 비장, 복수, 흉수 등이다. 임상에서 자주 EUS-FNA를 시행하는 예는 췌장암, 췌장 낭성종양, 폐암에서의 종격동 림프절, 식도암에서의 복강 림프절(celiac node), 점막하 종양, 작은 간 종괴, 종격동의 종괴 또는 림프절 등이 있다.
American Joint Committe on Cancer에서는 췌장 종괴의 생검이 필요할 때 가능하면 우선적으로 EUS-FNA를 권고하고 있다. 시술 전에는 내시경과 병변 사이에 출혈이 가능한 혈관이 있지 않은지를 도플러 검사로 미리 확인하여야 한다. 채취한 세포 조직은 슬라이드 위에 바로 옮기고 조직은 시술현장에서 세포병리의사가 다루는 것이 원칙이다. EUS-FNA의 진단 정확도는 병변 위치에 따라 70~90%로 알려져 있다. 병변에 EUS-FNA와 EUS-TCB를 동시에 시행하면 진단 정확도는 95%로 증가한다. 합병증은 0.3~6.3%로 보고되며 출혈과 감염이 있으나 대부분 경미하여 안전하게 시행할 수 있다. 혈관이 많은 종양은 출혈의 위험이 크며 시술 후 균혈증이나 감염은 매우 드물어 예방적 항생제는 낭성 병변이나 직장이나 대장을 통한 시술, proton pump inhibitor 복용 환자에서만 시행한다. 세침이 종양을 통과하면 드물지만 종양세포 전이의 가능성이 있다.
직립형 내시경초음파 유도하 Trucut 조직검사
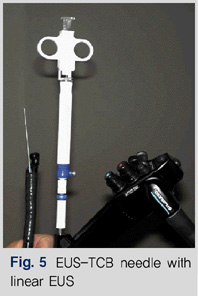
EUS-FNA는 세포 진단이므로 충분한 조직을 얻을 수 없다. 또한 혈액이나 양성 세포가 포함되면 감별진단이 어렵다. 또한 진단을 위해 충분한 조직이 필요한 림프종, 간질종양, 신경내분비종양, 고분화 췌장암에서는 진단이 어렵다. 직립형 내시경초음파 유도하 Trucut 조직검사(linear EUS-guided Trucut biopsy, EUS-TCB)는 cutting needle로 많은 조직을 잘라 얻는 방법으로 19 G, 18 mm의 비교적 큰 조직을 얻을 수 있다(Fig. 5).
바늘 삽입은 EUS-FNA 방법과 동일하나 Trucut 침은 직경이 두꺼워 십이지장 구부 아래에서는 시술이 어렵고 특히 시술 시에는 내시경과 바늘을 되도록 직선화하여야 한다. 절대적 금기는 접근이 불가능하거나 시술 시에 내시경과 병변 사이에 방해물이 있거나 혈액응고장애, 혈소판감소증이 있는 경우 등이다. 췌장 질환 중 자가면역 췌장염이나 만성비특이적 췌장염 진단은 EUS-FNA보다 EUS-TCB가 필요하다.
내시경초음파를 이용한 치료
내시경초음파를 이용한 치료에는 직립형 내시경초음파가 이용되며 EUS-FNA 침을 이용하여 병변에 도달한 후에 이 루트를 이용하여 시술을 하게 된다. 지금까지 임상에서 사용되는 치료법에는 복부 통증 치료에 사용되는 내시경초음파 유도하 복강신경얼기 차단술 혹은 신경박리술(EUS-guided celiac plexus block or neurolysis), 내시경초음파 유도하 췌장 가성낭종 및 농양 배액술(EUS-guided pancreatic pseudocyst and abscess drainage), 내시경초음파 유도하 췌담도 조영술(EUS-guided cholangiopancreatography) 및 배액술(EUS-guided drainage), 내시경초음파 유도하 주사요법(EUS-guided injection therapy), 내시경초음파 유도하 복강내 종양치료(EUS-guided tumor therapy), 내시경초음파 유도하 내시경 수술(EUS-guided endoscopic surgery), 내시경초음파 유도하 혈관조영술(EUS-guided angiography) 등이 있다.
현재 개발중인 내시경
현재 개발 중인 내시경 영상기술은 광유도형광분광경(light-induced fluorescence spectroscopy), 광확산분광경(light-scattering spectroscopy), Raman분광경, 3모드분광경(trimodal spectroscopy), 광간섭단층촬영(optical coherence tomography, OCT), 레이저주사공초점현미경(laser scanning confocal microscopy, LCM) 등이 있다.10) 광유도형광분광경은 조직내에 있는 fluorophore를 이용한 것으로 이는 특정 파장의 빛을 흡수하여 형광 빛을 발산하는 조직의 autofluorescence를 응용한 것이다. 악성과 양성 조직은 각기 발산하는 빛의 분광이 다르다. 광확산분광경은 조직에서 빛이 분사될 때 세포 핵의 크기와 개수에 따라 분사량이 다르다는 것을 이용한다. 이형성 세포는 특징적으로 핵이 크고 모여있다. 광간섭단층촬영(OCT)은 초음파영상의 B모드 같이 소화관의 단면상을 만드는데 초음파가 아닌 빛을 이용한 것이다. 빛을 사용하면 초음파보다 해상도는 좋아지는 반면 심달도는 감소한다. OCT는 실시간으로 조직의 고해상도 단면 영상을 만들 수 있다. 내시경의 부속채널에 optical probe를 넣어 영상을 만드는데 시간이 오래 걸리고 심달도가 낮은 문제점이 있다. 레이저주사공초점현미경(LCM)은 레이저를 이용하여 조직 표면 아래의 3차원 현미경 영상을 만들 수 있다. 시술 시간이 길고 조직에 수직으로 endomicroscope를 위치시켜야 하는 문제가 있다. 하지만 LCM은 점막층의 실시간 조직검사가 가능한 새로운 기술이다.
결론
소화기 질환의 진단과 치료에서 내시경은 최근에 가장 중요한 도구 중 하나이다. 소화기암의 진단에서 소화기내시경의 여러 가지 영상의 발전은 조직검사 이전에 병을 진단할 수 있는 optical biopsy의 개념에 근접해 있다. 그리고 1980년대 개발된 내시경초음파는 소화기의 영역을 위장관 뿐만 아니라 위장관 주위까지 확대하여 현재 국내에서도 EUS-FNA와 EUS-TCB가 널리 행해지고 있다. 또한 내시경적 용종절제술과 지혈치료, 내시경적 유두절개술(endoscopic sphincterotomy)로 시작된 내시경 치료는 현재 조기위암의 치료 뿐만 아니라 다양한 내시경초음파를 이용한 치료로 확대되고 있다.
- [부음]박현승 前 대한의사협회 총무이사 별세
- [인사]국경없는의사회, 자비드 압델모네임 신임 국제회장 취임 (9/5)
- [동정]삼성바이오에피스, 직업능력개발 관련 고용노동부 장관 표창
- [인사]보건복지부 과장급 전보 (9/3)
- [동정]대구가톨릭대병원 박기영 교수, 아시아-오세아니아 재활의학회 학술대회서 특별강연·연구발표
- [화촉]남궁승균 JW중외제약 홍보팀 매니저 (9/21)
- [인사]서울성모병원 직원인사(9/1)
- [동정]콜마비앤에이치, ‘한국ESG경영대상’ 중견기업 대상 수상
- [인사]알보젠코리아, 이욱세 신임 대표이사 취임 (9/1)
- [인사]가톨릭대 인천성모병원, 제22대 의무원장에 김종태 교수 선임
- [동정]삼성바이오에피스, 직업능력개발 관련 고용노동부 장관 표창
- [동정]대구가톨릭대병원 박기영 교수, 아시아-오세아니아 재활의학회 학술대회서 특별강연·연구발표
- [동정]콜마비앤에이치, ‘한국ESG경영대상’ 중견기업 대상 수상
- [동정]원텍, 탈모치료기 ‘헤어빔’으로 2025 올해의 브랜드 대상 7년연속 수상
- [동정]세노비스, 멀티비타민·키즈 비타민 ‘2025 올해의 브랜드 대상’ 수상
- [동정]충남대학교병원 강민웅 교수, 장영실상 수상
- [동정]원텍, ‘올리지오 키스’로 2025 올해의 브랜드 대상 2년연속 수상
- [동정]휴젤, ‘웰라쥬’ 2025 올해의 브랜드 대상 수상
- [동정]고대 구로병원 이의석 교수, 보건복지부장관 표창 수상
- [동정]GC녹십자, ‘2025 노사문화 우수기업’ 선정













