로슈 ‘알레센자’, 비소세포성폐암 1차 치료제 향한 행보
ALEX 연구 결과, 1차 티료제 '크리조티닙' 대비 우월한 효과 입증
- 김윤미 기자 kym@medifonews.com
- 등록 2017-06-22 05:40:00
 한국로슈의 ALK 양성 국소 진행성 또는 전이성 비소세포성폐암 치료제 ‘알레센자(성분명 알렉티닙염산염)’는 현재 이전에 ‘크리조티닙’으로 치료 경험이 있는 환자에서 2차 치료제로 사용되고 있다.
한국로슈의 ALK 양성 국소 진행성 또는 전이성 비소세포성폐암 치료제 ‘알레센자(성분명 알렉티닙염산염)’는 현재 이전에 ‘크리조티닙’으로 치료 경험이 있는 환자에서 2차 치료제로 사용되고 있다.
하지만 최근 6월 2일~6일까지(현지시간) 미국 시카고에서 개최된 미국임상종양학회(American Society of Clinical Oncology)에서 “진행성 비소세포성폐암 환자에서 알렉티닙과 크리조티닙의 비교 임상”인 ALEX 3상 연구 결과를 발표하며, 1차 치료제로서의 적응증 확대 가능성을 높였다.
ALEX 연구는 이전에 치료 경험이 없는 ALK 양성 진행성 비소세포성폐암 환자 303명을 대상으로 알렉티닙과 크리조티닙의 효과와 안전성을 비교하기 위해 31개국 161개 기관에서 진행된 무작위, 다기관, 오픈라벨 3상 임상이다.
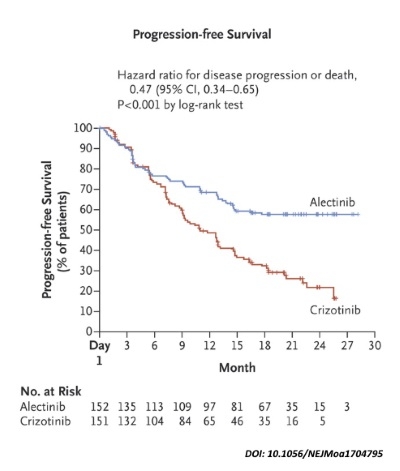 연구 결과 알렉티닙으로 치료받은 환자군에서 크리조티닙으로 치료받은 환자군보다 질병 악화와 사망 위험이 유의미하게 감소(53%)한 것으로 나타났다.
연구 결과 알렉티닙으로 치료받은 환자군에서 크리조티닙으로 치료받은 환자군보다 질병 악화와 사망 위험이 유의미하게 감소(53%)한 것으로 나타났다.
1차 종료점에서 크리조티닙 치료군의 연구자 평가 무진행 생존기간 중간값(mPFS)은 11.1개월(95% CI: 9.1-13.1 months)로 나타난 반면, 알렉티닙 치료군(95% CI: 17.7-not reached)은 아직 도달하지 않았다.
2차 종료점에서 독립검토위원회(independent review committee, IRC)가 평가한 알렉티닙 치료군의 무진행 생존기간 중간값은 25.7개월(95% CI: 19.9-not reached)로 크리조티닙 치료군의 10.4개월(95% CI: 7.7-14.6 months)보다 15.3개월이나 연장된 것으로 나타났다.
한편, 이번 연구에서의 알렉티닙 안전성 프로파일은 이전 연구들과 동일한 것으로 나타났다.
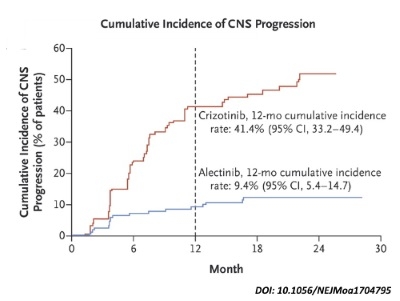 또한, 알렉티닙은 중추신경계(CNS)에서의 질병 진행 위험을 84%까지 감소시키는 것으로 나타났다.
또한, 알렉티닙은 중추신경계(CNS)에서의 질병 진행 위험을 84%까지 감소시키는 것으로 나타났다.
임상 설계 당시 중추신경계 전이 여부와 상관없이 임상 1년 후 중추신경계 질환 진행 누적률이 알렉티닙 치료군에서는 9.4%(95% CI: 5.4-14.7%), 크리조티닙 치료군에서는 41.4%(95% CI: 33.2-49.4%)로 나타난 것이다.
로슈에서 글로벌 신약개발을 총괄하고 있는 산드라 호닝(Sandra Horning) 의학부 부서장(CMO)은 “알레센자는 암의 진행 위험을 절반 이상으로 감소시켰으며, 뇌로의 암 전이와 진행 위험 또한 감소시키는 압도적인 효과를 보였다”며, “이번 연구 결과들은 적어도 1년에서 2년 이상 질병의 악화 없이 환자의 삶을 연장시키며 비소세포성폐암 치료 기준을 한 단계 향상시켰다”고 강조했다.
로슈는 이번 연구 결과들을 FDA를 포함한 전 세계 규제 당국에 제출할 예정이라고 밝혔다. 한편, FDA는 지난 2016년 9월 알레센자를 이전에 ALK 억제제로 치료 받지 않은 ALK 양성 진행성 비소세포성폐암 환자 치료를 위한 혁신의약품으로 지정한 바 있다.
이번 임상에서 비교 약물로 사용된 크리조티닙(제품명 잴코리(화이자)) 현재 국내에서 ALK 표적치료제 중 비소세포폐암 1차 치료에 보험급여가 적용되는 유일한 치료제다. 지난 1월 기존 2차 치료에서 1차 치료로 급여가 확대된 바 있다.
하지만 업계 관계자에 따르면, 크리조티닙으로 치료 받은 환자의 절반가량이 1년 안에 ALK 유전자 변이가 발생하여 내성을 나타내며, 많은 수에서 뇌전이가 진행되어 다른 치료 옵션이 필요하다는 의견이다.
이런 가운데 로슈의 알레센자가 1차 치료제인 크리조티닙 대비 월등히 우수한 효과를 입증하며 비소세포성폐암 치료의 새로운 장을 연 것이다.
알레센자는 ▲ALK에 고도로 선택적이고, ▲다양한 ALK 변이에 작용하며, ▲높은 전신 반응률, ▲우수한 CNS 효능, ▲우수한 내약성 프로파일을 식품의약품안전처로부터 인정 받으며 비소세포폐암 2차 치료제로 지난 4월 비급여 출시됐다.
아직 국내에서는 2차 치료제로도 급여 인정이 안된 상태지만, 로슈가 이번 ALEX 연구 결과를 바탕으로 전 세계 규제당국에 1차 치료제로서의 적응증 확대 신청하겠다 밝힌 만큼 국내에서의 알레센자 안착은 더욱더 속도가 붙을 것으로 예상된다.
- [부음]송봉규 부천 세종병원 중환자실장 장인상
- [부음]권경록 울산 나을한의원 원장 부친상
- [동정]제주대병원, 퇴원손상심층조사 공로 복지부장관상
- [동정]경상국립대병원 양정욱 교수 연구팀 논문, npj 디지털 메디슨 게재 및 BRIC '한빛사' 선정
- [동정]충남대병원 대전·충남권역심뇌혈관질환센터, 한글 점자의 날 기념식에서 감사패 수상
- [동정]고대 안산병원 박현지 전공의, 대한산부인과학회 최우수 포스터상 수상
- [동정]순천향대 문종호 부천병원장, 카자흐스탄 국립의대 명예교수 위촉
- [동정]인하대병원, 질병관리청장 표창
- [동정]고대 안산병원 이수교 교수, 대한심폐소생협회 젊은연구자상 수상
- [동정]고대 구로병원 최민주 교수, ‘제5회 아시아 폐렴구균 심포지엄’에서 ‘젊은과학자상’ 수상
- [인사]강동경희대학교병원 심계식 교수, 대한소아내분비학회 회장 취임
- [인사]고대 구로병원 이재관 교수, 대한산부인과학회 신임 이사장 선출
- [인사]일동생활건강 신임 대표에 박하영 상무 선임 (11/1)
- [인사]웰스바이오, 서석찬 신임 대표이사 선임
- [인사]대한전공의협의회 한성존 회장 당선
- [인사]동아쏘시오그룹 임원 인사 (11/1)
- [인사]전남대병원 이지범 교수, 대한피부과학회 제63대 차기 회장 공식 인준
- [인사]한림대성심병원 장대영 교수, 대한위암학회 신임 회장 취임
- [인사]서울약대 이정원 교수, 분자·세포생물학회 2027년 회장 당선
- [인사]고려의대 윤석준 교수, 제18대 대한예방의학회 이사장 선출
- [동정]제주대병원, 퇴원손상심층조사 공로 복지부장관상
- [동정]경상국립대병원 양정욱 교수 연구팀 논문, npj 디지털 메디슨 게재 및 BRIC '한빛사' 선정
- [동정]충남대병원 대전·충남권역심뇌혈관질환센터, 한글 점자의 날 기념식에서 감사패 수상
- [동정]고대 안산병원 박현지 전공의, 대한산부인과학회 최우수 포스터상 수상
- [동정]순천향대 문종호 부천병원장, 카자흐스탄 국립의대 명예교수 위촉
- [동정]인하대병원, 질병관리청장 표창
- [동정]고대 안산병원 이수교 교수, 대한심폐소생협회 젊은연구자상 수상
- [동정]고대 구로병원 최민주 교수, ‘제5회 아시아 폐렴구균 심포지엄’에서 ‘젊은과학자상’ 수상
- [동정]휴온스바이오파마, 2025 충청북도 ‘고용우수기업’ 수상
- [동정]칠곡경북대학교병원 하윤석 교수, 대한비뇨의학회 ‘국내논문 기초 최우수상’ 수상