[특별기획] ASCO 2018 핵심 요약 (2) – BMS·ONO '옵디보' 편
다양한 암종에서 여보이 및 타 약제와의 병용 탐구
- 김윤미 기자 kym@medifonews.com
- 등록 2018-06-20 05:50:00
지난 1편이 MSD ‘키트루다’였다면 2편에서 소개할 약물은 같은 항 PD-1 기전의 BMS·ONO ‘옵디보’다.
BMS·ONO 역시 이번 ASCO 2018에서 ‘옵디보’ 관련 연구 발표와 면역항암치료에서의 바이오마커 연구까지 약 20여 편의 연구 결과를 발표했다.

흑색종 3~4기 환자에서의 여보이 대비 우월성 입증
4일 흑색종/피부암 세션에서 발표된 3상 임상 CheckMate-238 연구 결과는 흑색종 치료에서 항 PD-1 기전 면역항암제의 최장기 추적관찰 연구다.
이 연구에서 옵디보는 절제술을 받은 3~4기의 광범위한 흑색종 환자군에서 여보이 대비 지속적이고 우월한 재발 없는 생존율을 입증했다. 옵디보는 이 환자군에서 활성대조군보다 우월성을 입증할 수 있는 유일한 면역항암 치료제다
CheckMate-238 연구는 절제술 후 재발 가능성이 높은 흑색종 3B/C기 혹은 4기 환자에서 옵디보와 여보이의 치료 효과와 안전성을 평가했다.
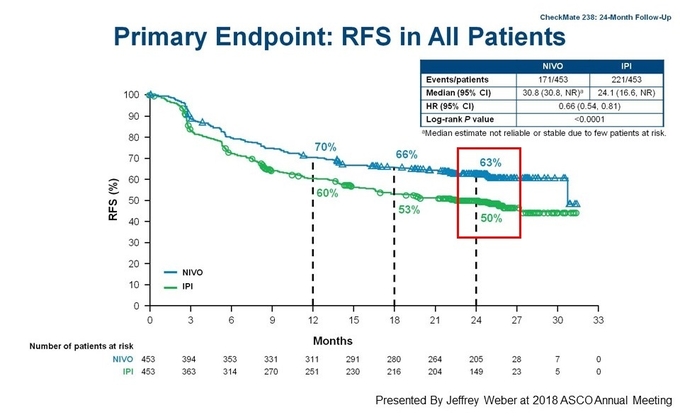
질병 단계와 BRAF 돌연변이 상태를 포함한 핵심 하위 그룹에서 최소 24개월간 추적 관찰한 결과, 옵디보는 지속적으로 재발 없는 생존율 62.6%을 나타내며 여보이의 50.2% 대비 개선된 효과를 보였으며, 사망률을 34% 감소했다(그림1).
뿐만 아니라 24개월간 이전과 다른 안전성 문제가 관찰되지 않았다. 옵디보는 이전에 18개월차 분석에서 여보이 대비 현저하게 낮은 이상반응 발생률을 입증한 바 있다.
이전 연구에서 이상반응으로 인한 투여 중단율은 옵디보군에서 9.7%, 여보이군에서 42.6%를 보였으며, 치료와 연관된 3/4단계 부작용 발생률은 옵디보에서 14.4%, 여보이에서 45.9%로 확연한 차이를 보였다.
뿐만 아니라 옵디보는 해당 연구에 참여한 ITT 환자에서 질병 단계, PD-L1 발현율, BRAF 변이 상태와 상관없이 여보이 대비 우월한 무재발생존율을 나타냈다(옵디보 62.6% 대 여보이 50.2%).
3B기 흑생종 환자에서 24개월차 무재발생존율은 옵디보 70.8% 대 여보이 60.7%, 3C기 환자에서는 옵디보 58.0% 대 여보이 45.4%, 4기 환자에서는 옵디보 58.0% 대 여보이 44.3%로 나타났다.
BRAF 변이 흑색종 환자에서 무재발생존율은 옵디보가 61.9% 대 여보이 51.7%, BRAF 정상형 흑색종 환자군에서는 옵디보 63.5% 대 여보이 46.2%로 나타났다.
CheckMate-238 연구의 수석연구원 제프리 웨버(Jeffrey S . Weber) 박사는 "면역항암 치료제들의 광범위한 사용으로 암 치료 환경이 바뀌었고, 연구의 발전으로 질병 재발을 예방하기 위해 흑색종에서 보조요법으로 이들 약물의 사용을 확대할 수 있었다"고 말하며, "보조요법으로서 PD-1 억제제를 가장 장기 추적한 이번 24개월 추적조사 결과는, BRAF 돌연변이 상태 및 흑색종의 다양한 단계에 걸쳐 옵디보의 혜택을 강력하게 뒷받침하고 있다"고 강조했다.
NSCLC 환자에서 ‘옵디보+화학요법’과 ‘옵디보+여보이’ 병용 평가
같은 날 ‘전이성 비소세포폐암’ 구두발표 세션에서 발표된 CheckMate-227 연구는 비소세포폐암 환자에서 ‘옵디보+여보이’ 병용과 ‘옵디보+화학요법’ 병용을 화학요법 단독 대비 평가한 3상 임상연구다.
종양의 조직학적 특성인 편평, 비편평과 관계없이 PD-L1 발현율이 1% 미만인 진행성 비소세포폐암 환자를 대상으로 연구를 진행했으며, 이날 발표된 결과는 CheckMate-227 연구의 1b 파트에 해당한다.
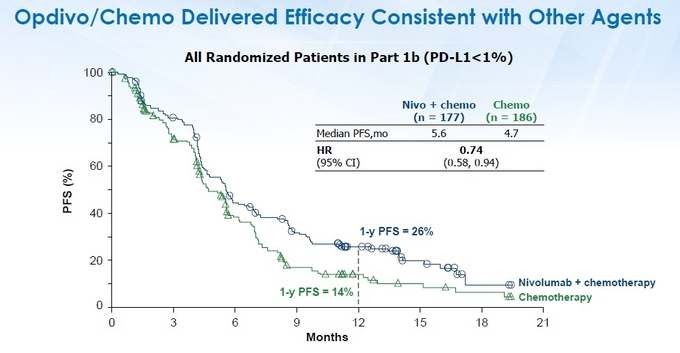
연구 결과, PD-L1 발현율이 1% 미만인 환자에서 옵디보+화학요법 병용군(177명)은 화학요법 단독군(186명) 대비 질병 진행 위험을 26% 감소시켰으며, 무진행생존기간을 개선하는 것으로 나타났다(그림2).
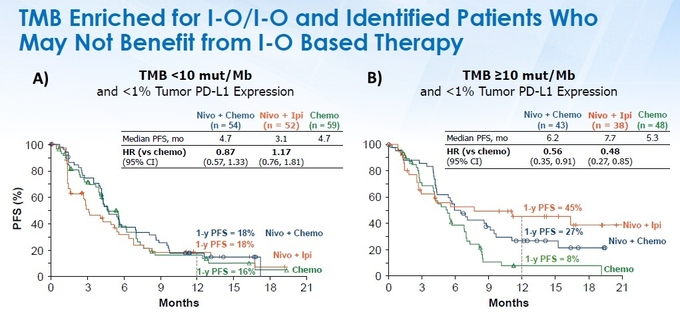
한편, 종양변이부담(TMB) 상태에 따른 ‘옵디보+여보이’ 및 ‘옵디보+화학요법’ 병용요법 데이터 또한 발표됐는데, TMB가 10 mut/Mb 이상이고 PD-L1 발현율이 1% 미만인 환자를 대상으로 한 분석 결과, 1년 무진행생존율 ‘옵디보+저용량 여보이’ 병용군(38명)이 45%, ‘옵디보+화학요법’ 병용군(43명)이 27%, 화학요법 단독군(48명)이 8%였다(그림3B).
객관적 반응률은 ‘옵디보+저용량 여보이’ 병용군이 36.8%, ‘옵디보+화학요법’ 병용군이 60.5%, 화학요법 단독군이 20.8%였다.
TMB가 10 mut/Mb 미만으로 낮으면서 PD-L1 발현율이 1% 미만인 환자인 경우, 1년 무진행생존율은 ‘옵디보+저용량 여보이’ 병용군(52명)과 ‘옵디보+화학요법’ 병용군(54명)이 18%, 화학요법 단독군(59명)이 16%였다(그림3A).
이번 연구에서 3~4등급 치료 관련 이상반응(TRAEs)은 ‘옵디보+저용량 여보이’ 병용군의 25%, ‘옵디보+화학요법’ 병용군의 52%, 화학요법 단독군의 35%에서 나타났다.
‘옵디보+저용량 여보이’ 병용군에서 가장 많이 발생한 3~4등급 치료 관련 이상반응은 간(8%), 위장관(3%), 내분비계(3%), 피부(3%), 설사(2%), 빈혈증(2%), 피로(1%), 무력증(1%), 구토(1%)였으며, ‘옵디보+화학요법’ 병용군에서는 빈혈증(17%), 호중구감소증(12%), 호중구 수 감소(10%), 피로(5%), 간(3%), 식욕감퇴(2%), 구토(2%), 위장관(2%), 설사(1%), 피부(1%), 내분비계(0.6%)였다.
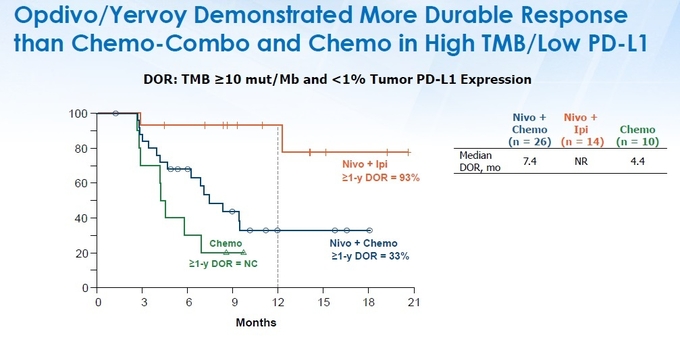
이번 임상시험 연구자이며 필라델피아 폭스체이스 암센터(Fox Chase Cancer Center)의 흉부종양내과장인 호세인 보르가이(Hossein Borghaei) 박사는 “두 면역항암제 간 병용요법과 면역항암제-화학요법 병용요법 데이터를 한 번에 확인할 수 있는 임상연구는 CheckMate-227이 최초”라며, “PD-L1이 발현되지 않은 폐암 환자의 1차 치료에서 옵디보+화학요법 병용요법은 화학요법 대비 무진행생존기간을 향상시켰으며, 지금까지 발표된 CheckMate-227의 다른 데이터와 종합해보면 종양변이부담 상태가 옵디보 기반의 병용요법과 임상적으로 유의미한 연관성이 있고, 종양변이부담이 높은 환자에서 ‘옵디보+저용량 여보이’ 병용요법의 효과가 장기적으로 나타난다는 것을 알 수 있다”고 설명했다(그림4).
BMS의 흉부종양부문 개발 책임자인 사빈 마이어(Sabine Maier) 박사는 “비소세포폐암 치료 환경이 계속 바뀌고 있는 와중에, CheckMate-227 연구의 옵디보 기반 병용요법 데이터는 면역항암제 연구개발에 의의를 더한다”고 말하며, “이를 통해 어떤 환자에서 면역항암제 병용요법의 치료효과를 기대할 수 있을지 확인하는 종양변이부담과 같은 예측적 바이오마커를 더 깊게 이해할 수 있다”고 강조했다.
진행성 신세포암 환자에서 ‘옵디보+저용량 여보이’ 병용
한편 4일 포스터 세션에서 발표된 CheckMate -214 연구는 치료 경험이 있는 진행성 신세포암 환자에서 ‘수니티닙’ 대비 ‘옵디보+여보이’ 병용요법을 평가한 3상 임상연구다.
참고로 이 환자군에서 면역항암제 간 병용요법으로 FDA의 허가를 받은 콤보는 ‘옵디보+저용량 여보이’가 최초이자 유일하다.
해당 연구에서 2년간 추적 관찰을 통해 환자로부터 보고된 결과치와 기저치와의 차이를 수니티닙 투여군과 비교 분석한 결과, 중등도 이상의 진행성 신세포암 환자에서 ‘옵디보+저용량 여보이’ 병용요법이 유의하고 지속적으로 환자의 질병 관련 증상 개선과 암 관련 삶의 질 향상에 이득을 가져다 주는 것으로 나타났다.
또한 이러한 이점은 ‘옵디보+저용량 여보이’ 투여 초기부터 관찰되었으며, 치료기간과 옵디보 유지치료 내내 유지된 것으로 나타났다.
해당 연구에서 미국종합암네트워크(NCCN)의 ‘암 치료의 기능적 평가 – 신장암 증상 지수(Functional Assessment of Cancer Therapy-Kidney Symptom Index 19, FKSI-19)’을 통해 삶의 질이 저하되기까지 걸린 시간(Time to Deterioration, TTD)을 평가한 결과, 2년 추적 관찰에서 ‘옵디보+저용량 여보이’ 병용군은 수니티닙 투여군보다 46% 낮은 수치를 기록했다.
또한, ‘옵디보+저용량 여보이’ 병용요법의 FKSI-19 평균 점수는 수니티닙 투여군 대비 3.55점 더 높았으며(1.65 vs -1.9, P <0.0001), 이는 ‘옵디보+저용량 여보이’ 병용군이 수니티닙 투여군 대비 질병 관련 증상, 치료 부작용 등과 관련된 삶의 질 데이터에서 우세하다는 것을 의미한다.
시카고 소재 노스웨스턴 페인버그의대 의료사회과학부 총괄 책임자인 데이비드 셀라(David Cella) 박사는 "CheckMate-214 연구를 통해 우린 이전에도 진행성 신세포암 환자에서 ‘옵디보+저용량 여보이’ 병용이 전체생존율, 객관적반응률 및 무진행생존율을 포함한 다양한 지표에서 이득이 있음을 확인한 바 있다”며, "우리은 이번 추가 분석을 통해 이 면역함암제 콤보가 환자의 질병 관련 증상 개선뿐만 아니라 신체적, 정서적 및 기능적 복지에 대한 긍정적인 변화를 가져왔다는 근거를 더했다"고 강조했다.
흑색종∙신장암∙요로상피암 환자 대상 ‘옵디보+NKTR-214’ 병용 탐구
한편 BMS는 이번 ASCO2018에서 치료 경험이 없는 4기 흑색종, 신장암, 요로상피암 환자를 대상으로 ‘옵디보’와 넥타 테라퓨틱스(Nektar Therapeutics)의 ‘NKTR-214’의 병용요법을 평가하기 위해 진행되고 있는 PIVOT 1/2상 임상의 기초 데이터(Preliminary Data)를 발표했다.
발표에는 임상 1상 용량 증량 단계에 등록된 환자들과 이후 임상 2상 용량 확대 코호트에 등록된 첫 환자들에서 나온 안전성, 효능, 생체지표 자료가 포함됐다.
현재 400명 이상의 흑색종, 신세포암, 요로상피세포암, 비소세포폐암 및 악성 유방암 환자가 2상 PIVOT 연구에 등록 중이다. 이날 발표된 내용은 흑색종, 신세포암, 요로상피세포암에 대한 1차 치료 연구에 관한 데이터다.
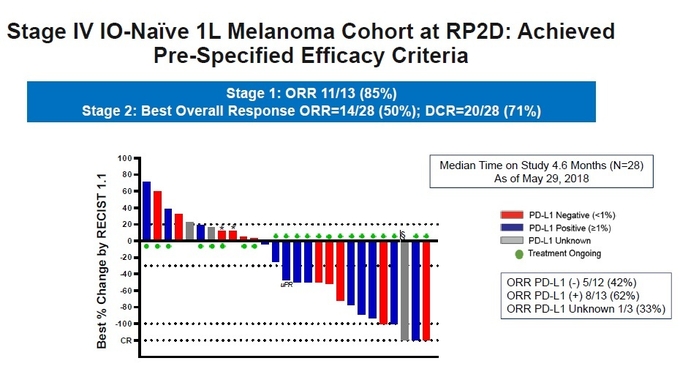
먼저, 치료 경험이 없는 4기 전이성 흑색종 환자의 1차 치료로서 ‘옵디보+ NKTR-214’ 병용은 1단계(Stage 1, 13명)에서는 85%(11/13)의 객관적반응률을, 2단계(Stage 2, 28명)에서는 50%(14/28)의 객관적반응률을 나타냈다(그림5).
또한, PD-L1 상태로 분류한 25명의 환자군에서 PD-L1 음성 환자군(12명)은 42%(5/12)의 객관적반응률을, PD-L1 양성 환자군(13명)은 62%(8/13)의 객관적반응률을 보였다. PD-L1 상태가 알려지지 않은 1명의 환자는 완전반응을 경험한 것으로 나타났다.
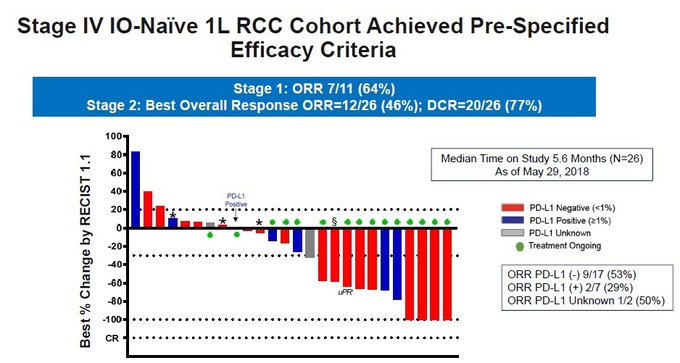
다음은 치료 경험이 없는 4기 전이성 신세포암 환자 대상 1단계(Stage 1, 11명)에서는 64%(7/11)의 부분반응률(PR)을 보였고, 2단계(Stage 2, 26명)에서는 46%(12/26)의 반응률을 보였다(그림6).
또한, PD-L1 상태로 분류한 24명의 환자군에서 PD-L1 음성 환자군(17명)은 53%(9/17)의 객관적반응률을, PD-L1 양성 환자군(7명)은 29%(2/7)의 객관적반응률을 보였다.
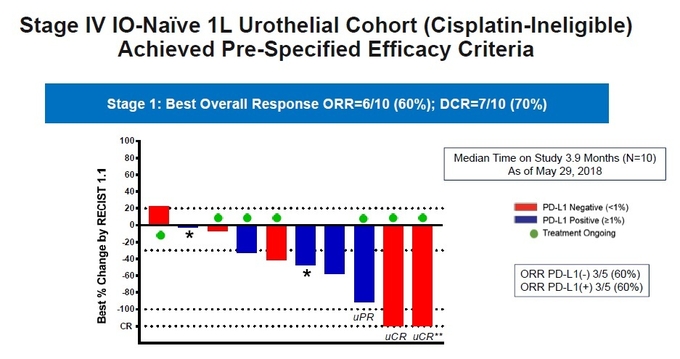
마지막으로 치료경험이 없는 4기 전이성 요로상피암 환자 대상 1단계(Stage 1, 10명)에서 60%의 객관적반응률을 보였으며, PD-L1 음성의 환자군(5명)과 양성 환자군(5명)은 모두 60%의 객관적반응률을 나타냈다(그림7).
회사 측은 “이번에 발표된 데이터 중 특히 PD-L1 음성 환자군에 대한 결과가 고무적이며, 이는 옵디보와 NKTR-214의 병용요법이 향후 암환자의 치료 혜택을 확대할 수 있다는 것을 반증한다”고 설명했다.
참고로 넥타 테라퓨틱스가 개발중인 ‘NKTR-214’는 CD122 단백질 편향 촉진제(biased agonist)의 일종으로 T세포 및 자연사멸세포들의 항암작용을 선택적으로 활성화시키는 면역 촉진제다.
 BMS와 넥타 테라퓨틱스는 지난 2월 면역항암제 프로그램 ‘NKTR-214’의 전략적 공동개발 및 글로발 마케팅을 진행하기 위한 제휴 계약을 체결하고, ‘NKTR-214’를 ‘옵디보’ 또는 ‘여보이’와의 복합요법제로 개발 중이다.
BMS와 넥타 테라퓨틱스는 지난 2월 면역항암제 프로그램 ‘NKTR-214’의 전략적 공동개발 및 글로발 마케팅을 진행하기 위한 제휴 계약을 체결하고, ‘NKTR-214’를 ‘옵디보’ 또는 ‘여보이’와의 복합요법제로 개발 중이다.
한편 BMS는 ‘NKTR-214’와 관련해 2018년 3분기 흑색종에서의 옵디보 단독 대비 ‘옵디보+NKTR-214’ 병용 효과를 평가하는 임상 등록을 진행할 계획이라고 밝혔으며, 방광암 등 타 암종에서의 탐고 또한 전개할 계획이라고 4일 진행된 ASCO2018 투자설명회를 통해 밝혔다.
(3)편에서 계속...
- [인사]보건복지부 인사(4/26)
- [인사]제약협회, 홍보전문위원장에 최천옥 한림제약 상무 재추대
- [인사]건일제약, 오인수 신임 마케팅본부장 영입
- [인사]삼천당제약 2024년 정기승진인사 (4/23)
- [인사]오태윤 강북삼성병원 교수, 의료기관평가인증원 제6대 원장 임명
- [인사]한미사이언스, 노용갑 부회장 영입
- [인사]사노피 배경은 대표, 한국 및 호주/뉴질랜드 제약 총괄 다국가 리드 선임
- [인사]연세대학교의료원 인사
- [인사]서울성모병원 오득영 교수, 대한미용성형외과학회 이사장 취임
- [인사]고대 안암병원 함병주 교수, 대한생물정신의학회 이사장 취임
- [동정]전북대병원 이선영 교수팀, 국제학술지 ‘Cancers’ 에 논문 게재
- [동정]암젠, 아동·청소년 생명과학 교육 캠페인 서울시장 표창 수상
- [동정]칠곡경북대병원 성인 수두증 클리닉, 30억원 치매극복 기술개발 과제 수주
- [동정]갑상선 수술 관련 비디오 후두경 통한 기관삽관 유용성 입증
- [동정]한국머크 바이오파마, ‘일∙가정 양립 우수 기업’ 선정
- [동정]고대 구로병원 송준영 교수, 질병청·국립보건연구원 학술연구용역 과제 선정
- [동정]일동후디스 하이뮨, 브랜드파워 단백질보충제 부문 2년 연속 1위
- [동정]서울성모병원 정미향 교수, 국제학술지 유럽예방심장학회지 부편집장 임명
- [동정]한올바이오파마, 국가산업대상 ‘연구개발’ 부문 수상
- [동정]제주대병원 연구팀, 국제학술지에 심장재활 논문 게재















