Pharma Focus
얀센 ‘리브리반트’, EGFR 엑손 20 삽입 변이 폐암에 승인된 최초의 치료제
- 노영희 기자 nyh2152@medifonews.com
- 등록 2022-06-13 17:06:59
 EGFR 엑손 20 삽입 변이 비소세포폐암은 EGFR 유전자 변이 중 세 번째의 유병률을 보이며, 전체 EGFR 변이의 약 12%를 차지한다.
EGFR 엑손 20 삽입 변이 비소세포폐암은 EGFR 유전자 변이 중 세 번째의 유병률을 보이며, 전체 EGFR 변이의 약 12%를 차지한다. 그러나 그간 승인된 치료제가 없었고, EGFR 타이로신 키나아제 억제제(Tyrosine Kinase Inhibitor, 이하 TKI)와 같은 기존 표적 치료제에 제한적인 효능을 보여 환자들의 예후가 좋지 않았다.
때문에 EGFR 엑손 20 삽입 변이 비소세포폐암 환자의 생존율 개선을 위해 보다 효과적이고 내약성 높은 표적 치료제가 필요하다는 의견이 꾸준히 제기됐는데, ‘리브리반트’의 등장으로 효과적인 치료 옵션이 부재한 EGFR 엑손 20 삽입 변이 비소세포폐암 환자에게 새로운 치료 기회를 제공할 수 있게 됐다.
한국얀센이 출시한 리브리반트TM주 (성분명 아미반타맙)는 EGFR 엑손 20 삽입 변이 비소세포폐암 치료에 승인된 최초의 완전 인간유래 이중특이적 항체다.
백금 기반 화학요법 치료 중 또는 치료 이후 질병이 진행된 EGFR 엑손 20 삽입 변이가 있는 국소 진행성 또는 전이성 비소세포폐암 환자의 치료를 적응증으로 허가됐다.
리브리반트는 활성 및 저항성 EGFR 변이와 MET 변이 및 증폭을 보이는 종양세포를 표적하도록 면역세포를 지시하는 저-푸코스 (low-fucose), 완전 인간유래 IgG1 기반 EGFR-MET 이중특이적 항체로 해당 계열 내 최초(first-in-class)의 약제다. 새로운 작용 기전으로 종양 성장을 억제하고 종양 세포의 사멸을 유도한다.
또 NK 세포(NK cells), 단핵구(monocytes), 대식세포(macrophages)를 동원하며, 면역을 활성화한다. 리브리반트는 리간드 결합을 차단하고 EGFR과 MET의 분해를 향상시킴으로써 EGFR과 MET 신호기능을 방해하며, 이로 인해 종양의 성장과 진행을 방지한다.
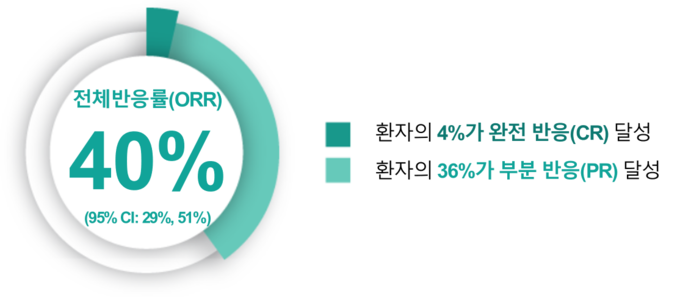
리브리반트 단독요법은 백금 기반 화학요법 치료 중 또는 치료 이후에 질병이 진행된 EGFR 엑손 20 삽입 변이 비소세포폐암 환자에서 40%의 전체반응률(ORR)이 확인됐다.
리브리반트의 국내 허가는 국소 진행성 또는 전이성 비소세포폐암 환자에서 리브리반트 단독요법의 안전성 및 유효성을 평가한 1상 임상시험 ‘CHRYSALIS’의 결과에 기반해 이뤄졌다.
CHRYSALIS 연구 결과, 리브리반트 단독요법군의 전체반응률(ORR)은 40%(95% CI: 29 – 51)였다. 참여 환자의 4%가 완전 반응(CR)을 보였으며, 36%가 부분 반응(PR)을 달성했다. 반응지속기간(DOR) 중앙값은 11.1개월 (95% CI: 6.9, Not Estimable)였다.
임상연구 결과를 근거로 미국종합암네트워크(National Comprehensive Cancer Network, NCCN) 가이드라인에서도 EGFR 엑손 20 삽입 변이 비소세포폐암 환자의 백금기반 화학요법 이후 치료법 중 하나로 리브리반트를 권고하고 있다.
CHRYSALIS 연구는 국소 진행성 또는 전이성 비소세포폐암 환자에 대한 리브리반트의 안전성과 유효성을 평가하기 위해 수행된 다기관, 라벨 공개, 복수 코호트 임상시험이다.
기존의 표준적인 검사법으로 EGFR 엑손 20 삽입 변이를 가진 것으로 진단됐으며, 백금기반 화학요법 진행 중 또는 이후에 질병이 진행한 국소 진행성 또는 전이성 비소세포폐암 환자 81명을 대상으로 유효성을 평가했다. 추적기간 중앙값은 9.7개월이다.
임상시험의 주요 목표는 눈가림된 독립적 중앙 검토위원회(Blinded Independent Central Review, BICR)가 평가한 고형암 반응평가 기준(RECIST v1.1)에 따른 전체반응률(ORR) 평가였다. 추가 효능 분석을 위해 반응지속기간(DoR)도 함께 평가했다.
80kg 미만인 환자에게는 이 약 1050mg, 80kg 이상인 환자에게는 이 약 1400mg을 처음 4주간은 주 1회 정맥투여했다. 이후에는 질병이 진행하거나 수용하기 어려운 독성이 나타날 때까지 2주에 1회 이 약을 투여했다.
리브리반트는 임상연구를 통해 백금 기반 화학요법 치료 중 또는 치료 이후에 질병이 진행된 EGFR 엑손 20 삽입 변이 비소세포폐암 환자에서 확실하고 지속적인 반응 및 관리 가능한 수준의 안전성 프로파일을 보였다.
임상연구에서 보고된 가장 흔한 이상반응(≥20%)은 발진(84%), 주입관련반응(64%), 손발톱주위염(50%), 근골격 통증(47%), 호흡곤란(37%), 오심(36%), 피로(33%), 부종(27%), 구내염(26%), 기침(25%), 변비(23%), 구토(22%)였다.
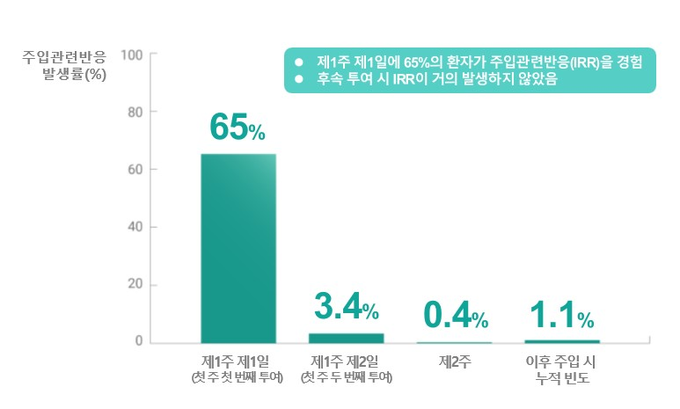
제1주 제1일에 65%의 환자가 주입관련반응(IRR)을 경험했으며, IRR은 대부분 1,2 등급이었고 후속 투여 시에는 거의 발생하지 않았다. 모니터링 및 예방 조치가 IRR 완화에 도움이 되는 것으로 나타났다.
- [동정]제주대학교병원 강현식·박경기 교수, 암예방 공로로 보건복지부장관 표창
- [동정]영남대병원 허민구 교수, 대한안과학회 '율산학술상' 수상
- [동정]건양대병원 김하영 전공의, 국제췌담도학회 ‘우수 구연상’
- [동정]고대 안암병원 이형래 교수, 대한정형외과 스포츠의학회 춘계학술대회 우수구연상 수상
- [동정]인천성모병원 이정훈 교수, ‘대한유방갑상선외과의사회 우수연제상’ 수상
- [인사]동화약품, 신용재 중선파마 호치민 지사장 선임
- [인사]건강보험심사평가원 홍승권 신임 원장 임명
- [동정]서울대병원 박중신 교수, 제54회 보건의 날 ‘황조근정훈장’ 수훈
- [동정]이대목동병원 유선아 전임의, 소화기기능성질환·운동학회 ‘젊은 연구자상’ 수상
- [인사]고대 안산병원 신승용 교수, 순환기의공학회 이사장 취임
- [인사]동화약품, 신용재 중선파마 호치민 지사장 선임
- [인사]건강보험심사평가원 홍승권 신임 원장 임명
- [인사]고대 안산병원 신승용 교수, 순환기의공학회 이사장 취임
- [인사]순천향대 부천병원 문종호 교수, ‘제19대 대한췌장담도학회 이사장’ 취임
- [인사]SK바이오, R&D 실행력 강화 위해 연구지원조직 정비 및 핵심인재 영입
- [인사]화순전남대병원 김인영 교수, 대한정위기능신경외과학회장 선임
- [인사]원광대병원 김정우 교수, 대한견주관절학회 제34대 회장 취임
- [인사]일동제약그룹 정기승진인사 (4/1)
- [인사]한국산텐제약, 신임 대표이사에 김진희 대표 선임 (4/1)
- [인사]일동제약, 새 R&D 본부장 박재홍 사장 선임
- [동정]제주대학교병원 강현식·박경기 교수, 암예방 공로로 보건복지부장관 표창
- [동정]영남대병원 허민구 교수, 대한안과학회 '율산학술상' 수상
- [동정]건양대병원 김하영 전공의, 국제췌담도학회 ‘우수 구연상’
- [동정]고대 안암병원 이형래 교수, 대한정형외과 스포츠의학회 춘계학술대회 우수구연상 수상
- [동정]인천성모병원 이정훈 교수, ‘대한유방갑상선외과의사회 우수연제상’ 수상
- [동정]서울대병원 박중신 교수, 제54회 보건의 날 ‘황조근정훈장’ 수훈
- [동정]이대목동병원 유선아 전임의, 소화기기능성질환·운동학회 ‘젊은 연구자상’ 수상
- [동정]가정의학과의사회 유승호 공보이사, 보건복지부 장관상 수상
- [동정]경북대병원 김혜정 연구교수·박준석 교수 연구팀, 대한대장항문학회 ‘우수포스터상’ 수상
- [동정]길병원 노영 교수, 치매 연구 공로, 보건의 날 맞아 복지부 장관 표창













