-

스트레스에 의한 우울 증상 유발 억제하는 내재적 기전 규명
고려대학교 의과대학(학장 윤영욱) 해부학교실 김현 교수팀이 고삐핵 미량아민 신경망 제어 및 우울 행동 분석 연구를 통해 스트레스에 의한 우울 증상 유발을 억제하는 신호전달계의 내재적 기전을 규명했다. 지속적인 스트레스는 우울 증상을 유발하는 것으로 알려져 있다. 스트레스는 외측고삐핵(lateral habenula)의 글루탐산성 신경세포의 활성을 촉진해 주내측피개핵 GABA성 신경세포를 활성화하고, 이는 도파민 신경세포의 활성 억제로 이어져 우울 증상을 유발한다. 그러나 일상적인 스트레스도 외측고삐핵 글루탐산성 신경세포의 활성화를 유발함에도 우울 증상이 발생하지 않는 현상을 두고, 많은 연구자들이 우울 증상 유발을 상쇄시키는 내재적 시스템의 존재 가능성을 제시했지만 현재까지 명확하게 밝혀지지 않았다. 이를 규명하기 위해 김현 교수 연구팀은 고삐핵 미량아민 신경망 제어 및 우울 행동 분석을 통해 미량아민 신호전달계와 우울 증상 유발의 밀접한 연관성을 분석했다. 스트레스 기반 우울증 동물모델 고삐핵에서 미량아민을 생산하는 AADC (L-amino acid decarboxylase) 유전자 발현이 특이적으로 감소하는 것을 관찰한 후, 인위적으로 고삐핵에서 AADC
- 이형규 기자
- 2023-08-01 16:58
-

신경전달물질 분비 조절하는 ‘칼슘채널’ 원리 규명
신경세포간의 신호전달에 중요한 칼슘채널의 조절 메커니즘이 밝혀졌다. DGIST 뇌과학과 서병창 교수 연구팀은 신경세포 말단에서 신경전달물질의 분비를 조절하는 중요한 단백질인 ‘전압의존성 칼슘채널’의 활성에 대한 분자적 기전을 규명했다고 23일 밝혔다. 서병창 교수 연구진은 다양한 수용체 및 이온채널들의 활성에 대한 PIP2의 분자적 기전에 대해 연구해왔다. 특히 연구진은 전압의존성 칼슘채널의 보조 소단위체인 β2 단위체의 세포막 결합 유무에 따라 칼슘채널의 PIP2에 대한 민감도가 달라짐을 규명한 바 있다. 이러한 연구를 바탕으로 본 연구에서는 β2 단위체의 세포막 결합 유무에 따라서 PIP2가 어떻게 CaV2.2의 활성을 다르게 조절하는지에 대한 원리를 분자적 수준에서 규명하고자 연구를 실시했다. 연구팀은 유전자 재조합을 통해 CaV2.2 채널과 β2 단위체의 다양한 변이 모델들을 만들어 전기 생리학 기법으로 확인했다. 그 결과, CaV2.2 채널에서 β2 단위체가 결합하고 있는 ‘I-II loop’와 전압감지 도메인 중 하나인 ‘S4II’에 PIP2가 각각 결합하여 채널의 활성을 조절한다는 것과 β2 단위체의 세포막 결합 유무에 따라 I-II loop에
- 김민준 기자
- 2022-11-23 09:07
-
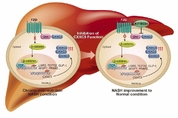
씨케이리제온, 윈트신호전달계 제어하는 경구용 NASH 치료제 개발
조직재생 신호전달 제어물질을 개발하는 ㈜씨케이리제온(대표이사 최강열; 연세대 생명공학과 교수 겸임)이 대사질환에서 낮아져 있는 윈트신호전달계(Wnt signaling pathway)를 회복시켜 작동하는 경구용 비알코올성 지방간염(NASH) 혁신형 신규물질을 개발했다고 밝혔다. 연구진은 개발 결과를 최근 16일에 실험분자의학(Experimental & Molecular Medicine, 영향력지수 12.178)에 온라인 게재했다(제 1저자 연세대학교 서설화 박사, 교신저자 최강열 교수, 논문 링크 :https://www.nature.com/articles/s12276-022-00851-8). 비알코올성 지방간염은 여러 복잡한 병리기전을 가진 대사 장애로 인해 발생하는 만성 간 질환으로 비만 및 당뇨병 환자에서 볼 수 있는 질환이다. 하지만 NASH 치료제는 아직 전무하며 치료제를 개발하기 위해 국내외 제약 바이오 기업들이 치열한 경쟁을 하고 있다. NASH 치료는 간 경변 및 후속 간세포 암종(HCC)으로 진행되지 않도록 예방이 필요한 만큼 의학적 미충족 수요가 높다. 연구진은 윈트신호전달계가 NASH 유발 마우스뿐만 아니라 대사질환을 앓고 있는 NAS
- 이형규 기자
- 2022-09-21 07:00
- [인사]조선대병원 임동훈 교수, 대한요로생식기감염학회 회장 선출
- [인사]보건복지부 인사(4/26)
- [인사]최광훈 회장, 건강기능식품이사에 이형우 약사 선임 (4/24)
- [인사]제약협회, 홍보전문위원장에 최천옥 한림제약 상무 재추대
- [인사]건일제약, 오인수 신임 마케팅본부장 영입
- [인사]삼천당제약 2024년 정기승진인사 (4/23)
- [인사]오태윤 강북삼성병원 교수, 의료기관평가인증원 제6대 원장 임명
- [인사]한미사이언스, 노용갑 부회장 영입
- [인사]사노피 배경은 대표, 한국 및 호주/뉴질랜드 제약 총괄 다국가 리드 선임
- [인사]연세대학교의료원 인사
- [동정]현대약품, 대한산업안전협회 무재해 11배수 달성 인증패 수상
- [동정]셀트리온, 근로자 건강증진활동 우수사업장 선정
- [동정]환인제약, 제26회 환인정신의학상 시상
- [동정]전북대병원 이선영 교수팀, 국제학술지 ‘Cancers’ 에 논문 게재
- [동정]암젠, 아동·청소년 생명과학 교육 캠페인 서울시장 표창 수상
- [동정]칠곡경북대병원 성인 수두증 클리닉, 30억원 치매극복 기술개발 과제 수주
- [동정]갑상선 수술 관련 비디오 후두경 통한 기관삽관 유용성 입증
- [동정]한국머크 바이오파마, ‘일∙가정 양립 우수 기업’ 선정
- [동정]고대 구로병원 송준영 교수, 질병청·국립보건연구원 학술연구용역 과제 선정
- [동정]일동후디스 하이뮨, 브랜드파워 단백질보충제 부문 2년 연속 1위















