암, HIV, 당뇨, 코로나19…5월 다양한 약품 특허 등재
암 치료제 최다…C형간염, 천식∙알레르기, 아토피 치료제도 특허
- 노영희 기자 nyh2152@medifonews.com
- 등록 2022-06-08 05:53:28
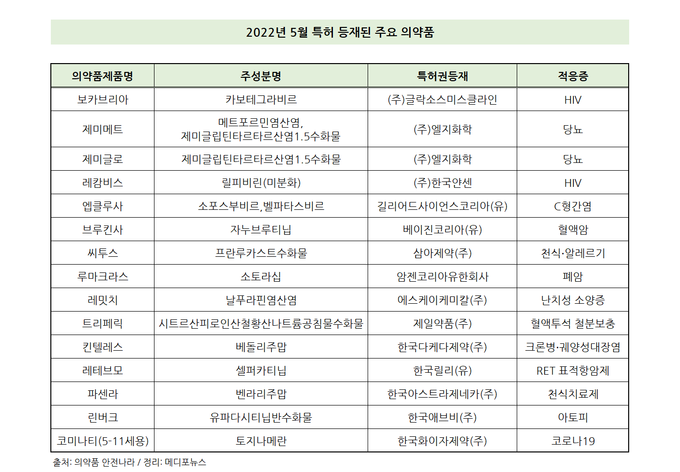
식품의약품안전처의 의약품 안전나라를 통해 확인한 결과 5월 특허 등재에 성공한 의약품이 총 39개 품목으로 나타났다. 이 중 용량, 제형 등 동일한 제품에 대한 여러 특허들을 제외하면 총 15개 의약품에 대한 특허 등재됐다.
특히 이번 허가에서는 암 치료제, HIV 주사, 당뇨약, 코로나19 백신 등 유의미한 제품들이 다수 포함돼 이번 특허 허가의 의미를 더했다.
베이진코리아의 혈액암 치료제 ‘브루킨사 80mg(성분명 자누브루티닙)’는 지난 2월 △이전에 한 가지 이상의 치료를 받은 적이 있는 외투세포 림프종(MCL) 성인 환자 단독요법 △발덴스트롬 마크로글로불린혈증(WM) △이전에 한 가지 이상의 치료를 받은 적이 있는 발덴스트롬 마크로글로불린혈증(WM) 성인 환자 단독요법에 대해 허가를 받았다.
이 중에서도 지난 4월에는 암질환심의위원회에서 ‘이전에 한 가지 이상의 치료를 받은 적이 있는 발덴스트롬 마크로글로불린혈증(WM) 성인 환자에서의 단독요법’에 대해 급여 심의를 통과하기도 했다.
브루킨사는 임상 2상만으로도 국내 허가된 만큼, 현재는 1차 치료제로 사용하기 위한 임상 3상 시험이 진행되고 있다.
암젠의 KRAS G12C 변이 국소진행성 또는 전이성 비소세포폐암 치료제 ‘루마크라스정120mg (소토라십)’는 지난 2월에 식약처 허가를 받은 제품이다. KRAS 표적 치료제 최초로 이전에 적어도 한 번의 치료를 받은 적이 있는 KRAS G12C 변이 국소 진행성 또는 전이성 비소세포폐암(NSCLC) 성인환자를 대상으로 허가됐다.
허가의 기반이 된 CodeBreaK100 임상 2상 연구에서는 환자군에서 완전관해와 부분관해를 포함한 객관적 반응률이 36%(n=124, 95% CI: 28-45)로 나타났다. 전체 치료 환자군의 82.3%에서 종양 수축이 관찰됐으며, 반응을 보인 전체 환자의 최대 종양 수축률 중앙값은 60%로 일관되게 높은 치료 효과를 보였다.
또한 해당 임상 연구의 1/2상에 대해 2년 장기 유효성과 안전성 결과를 살펴본 결과 완전관해, 부분관해를 포함한 객관적 반응률은 40.7%, 반응지속기간 중앙값은 12.3개월이었으며 질병조절율은 83.7%였다.
무진행생존기간 중앙값은 6.3개월, 전체생존기간은 12.5개월로 확인됐으며 치료 2년 시점에 전체 연구 참여 환자의 32.5%가 생존해 있는 것으로 나타났다. 장기 추적에서 기존에 없었던 새로운 이상반응에 대한 보고는 없었던 것으로 확인됐다.
릴리의 RET 표적항암제 ‘레테브모캡슐80mg(성분명 셀퍼카티닙)’은 3월 ▲전이성 RET 융합-양성 비소세포폐암 성인 환자 ▲전신요법을 요하는 진행성 또는 전이성 RET-변이 갑상선 수질암이 있는 성인 및 만 12세 이상 소아 환자를 대상으로 허가됐다.
또 ▲방사선 요오드에 불응하고, 이전 소라페닙 및/또는 렌바티닙의 치료 경험이 있으며 전신요법을 요하는 진행성 또는 전이성 RET 융합-양성 갑상선암 성인 환자를 위한 치료제로도 승인됐다.
허가는 RET 변이가 있는 진행성 혹은 전이성 고형암 환자 702명을 대상으로 진행된 LIBRETTO-001 임상 연구를 기반으로 이뤄졌다.
백금 기반 항암화학요법 치료 경험이 없는 RET 융합-양성 비소세포폐암 환자군에서 객관적 반응률은 85%(95% CI, 70-94)였다. 추적 기간(중앙값 7.4개월) 동안 79%에서 지속적인 반응을 보여 반응지속기간은 중앙값에 도달하지 않았다.
백금 기반 항암화학요법 치료 경험이 있는 환자군에서는 객관적 반응률은 64%(95% CI, 54-73), 반응지속기간 중앙값은 17.5개월(95% CI, 12.0-NE)로 확인됐다.
비소세포폐암 2차 평가변수로 중추신경계 전이 환자의 객관적 반응률을 별도로 평가한 결과 백금 기반 항암화학요법 치료 경험이 있고 뇌전이 부위의 측정이 가능한 RET 융합-양성 비소세포폐암 환자 11명 중 10명에서 중추신경계 객관적 반응이 확인됐다.
이전에 반데타닙 및/또는 카보잔티닙 치료 경험이 없는 RET-변이 갑상선 수질암 환자군에서 레테브모의 객관적 반응률은 73%(95% CI, 62-82), 완전 반응 비율은 11%였으며, 반응지속기간의 중앙값은 22.0개월(95% CI, NE-NE)이었다.
반데타닙 및/또는 카보잔티닙 치료 경험이 있는 환자군에서는 객관적 반응률은 69%(95% CI, 55-81)였고, 추적 기간 동안 84%의 환자가 지속적인 반응을 보여 반응지속기간은 중앙값에 도달하지 않았다.
소라페닙 및/또는 렌바티닙 치료 경험이 있는 RET 융합-양성 갑상선암 환자군에서 레테브모의 객관적 반응률은 79%(95% CI, 54-94), 반응지속기간의 중앙값은 18.4개월(95% CI, 7.6-NE)이었다. 주요 2차 평가변수 중 하나인 무진행생존기간 중앙값은 20.1개월(95% CI, 9.4-NE)로 확인됐다.
요즘 같은 때에 큰 역할을 해내고 있는 화이자의 코로나19 mRNA 백신 ‘코미나티주0.1mg/mL (토지나메란)’은 5-11세용에 대한 특허를 등재했다.
코미나티주0.1㎎/㎖(5-11세용)는 5~11세의 코로나19 예방 목적으로 美 화이자가 개발∙생산한 mRNA 백신이다. 기존에 허가된 ‘코미나티주’, ‘코미나티주0.1㎎/㎖’과 유효성분(토지나메란)은 같지만 1회 접종 시 투여량은 1/3(10㎍)에 그친다.
식약처는 코미나티주0.1㎎/㎖(5-11세용) 29만9000회분에 대해 검정시험을 수행하고 제조사의 제조∙시험 자료를 검토한 결과 효과성, 안전성, 품질을 확인했으며, 기준에 적합해 3월 국가출하 승인을 결정했다.
LG화학는 복제약 출시를 앞두고 있는 시점에서 자사 당뇨약 ‘제미메트서방정50/1000밀리그램(성분명 메트포르민염산염, 제미글립틴타르타르산염1.5수화물)’과 제미글로정50밀리그램(성분명 제미글립틴타르타르산염1.5수화물)에 대해 특허 등재에 성공했다.
HIV 치료제에서는 GSK(글락소스미스클라인)가 ‘보카브리아주(성분명 카보테그라비르)’를, 얀센이 ‘레캄비스주사(성분명 릴피비린)’를 특허 등재시켰다.
이외에도 C형간염, 천식∙알레르기, 난치성 소양증, 크론병∙궤양성대장염, 아토피 등 다양한 적응증을 토대로 한 의약품들이 5월 동안 허가됐다.
- [동정]아주대병원 김장희 교수, 제19회 암 예방의 날 보건복지부 장관 표창 수상
- [인사]황덕기 인천성모병원 영상의학팀장, 대한방사선사협회 인천광역시회 회장 당선
- [동정]배현진 프로메디우스 대표, KIMES 2026 식약처 처장 표창 수상
- [동정]국립중앙의료원, ‘제19회 암 예방의 날’ 보건복지부장관 표창 수상
- [동정]고대 구로병원 허윤정 교수, 대한외과술기연구회 춘계학술대회서 ‘최우수상’ 수상
- [부음]정주환 스마일 이비인후과 원장 부친상
- [부음]황정한 상주성모병원 이사장 장인상
- [동정]유비케어, 김진태 대표 복지부 장관 표창 수상
- [인사]동남권원자력의학원, 정형외과 장효석 과장 초빙
- [동정]서울부민병원 박성철 센터장, 아시아태평양 경추연구학회 베스트 논문상 수상
- [인사]황덕기 인천성모병원 영상의학팀장, 대한방사선사협회 인천광역시회 회장 당선
- [인사]동남권원자력의학원, 정형외과 장효석 과장 초빙
- [인사]대원제약 정기 승진 인사 (3/1)
- [인사]CSL, 한국 법인에 황세은 신임 대표 선임
- [인사]충북대병원 최미영 교수, 제18대 한국사시소아안과학회 회장 선출
- [인사]질병관리청 공무원 과장급 전보 (3/16)
- [인사]식약처 국·과장급 인사발령 (3/16)
- [인사]강동경희대학교병원 김동환 교수, 대한암재활학회 차기 회장 선출
- [인사]경희대학교병원 백종우 교수, 한국자살예방협회 회장 취임
- [인사]단국대병원 박재석 교수, 대한결핵 및 호흡기학회 회장 취임
- [동정]아주대병원 김장희 교수, 제19회 암 예방의 날 보건복지부 장관 표창 수상
- [동정]배현진 프로메디우스 대표, KIMES 2026 식약처 처장 표창 수상
- [동정]국립중앙의료원, ‘제19회 암 예방의 날’ 보건복지부장관 표창 수상
- [동정]고대 구로병원 허윤정 교수, 대한외과술기연구회 춘계학술대회서 ‘최우수상’ 수상
- [동정]유비케어, 김진태 대표 복지부 장관 표창 수상
- [동정]서울부민병원 박성철 센터장, 아시아태평양 경추연구학회 베스트 논문상 수상
- [동정]원광대병원, 메디컬 코리아 글로벌 헬스케어 유공 포상 대통령 표창 수상
- [동정]신신파스 아렉스, 2026 K-BPI 소염진통제 부문 8년 연속 1위
- [동정]한독여의사학술대상 수상자로 김봉옥 뿌리요양병원 명예원장 선정
- [동정]SK바이오-IVI, 美 오렌스타인 교수 등 ‘2026 박만훈상’ 수상자 선정 발표













