골다공증치료제 제네릭, 제약사 개발대상 1순위
식약청, 3/4분기 생동성시험계획서 승인현황 분석
- 이현경 기자 hk00@medifonews.com
- 등록 2011-10-20 10:29:37
현재까지 골다공증 치료제인 이반드론산나트륨의 제네릭 개발에 대한 제약사의 관심이 가장 높은 것으로 확인됐다.
최근 식약청에 따르면 2011년 3/4분기 생동성시험계획서 승인현황을 분석한 결과, 총 107건이 승인됐다. 이중 골다공증 치료제인 이반드론산나트륨의 제네릭 개발을 위한 승인이 23건으로 가장 많았다.
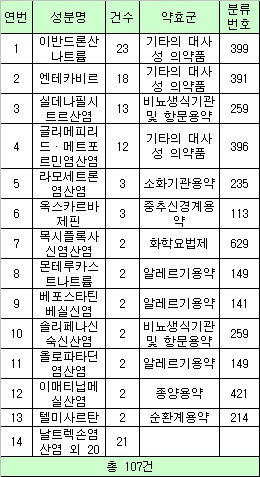
3분기에 성분별로 가장 많이 승인된 품목은 골다공증 치료제인 ▲이반드론산나트륨 (23건) ▲엔테카비르 (18건) ▲실데나필시트르산염 (13건) ▲글리메피리드·염산메트포르민염산염 복합제 12건(서방성제제) 순이다.
또 3분기에 생동성계획서를 처음 승인받은 성분을 살펴보면 ▲베포타스틴베실산염 ▲솔리페나신숙신산염 ▲에카베트나트륨 ▲엔타카폰 ▲발사르탄·암로디핀베실산염 복합제 등으로 나타났다.
이번 3/4분기 생동성승인건수는 119건이었던 작년에 비해 다소 감소한 수치다. 이처럼 승인건수는 지난 2009년 152건으로 집계된 이후 해마다 줄어들고 있는 추세다.
이는 재심사 기간이 만료된 리리카캡슐(프레가발린), 아마릴엠정(글리메피리드·메트포르민염산염)의 제네릭의약품 개발이 지난해와 올 상반기에 완료됐기 때문이다. 이 밖의 다른 주요품목들은 내년 상반기에 재심사 및 특허가 만료된다.
식약청 관계자는 “앞으로는 제약업계가 제네릭의약품 개발동향을 신속히 알 수 있도록 분기별로 생동성시험 계획성 승인현황을 분석해 발표할 예정”이라고 설명했다.
- [동정]한국아스트라제네카 대외협력, 한국보건산업진흥원장 표창 수상
- [인사]에스디생명공학, 신임 대표이사에 대원제약 백인영 본부장 선임
- [동정]충북대학교병원 문형철 박사, 대한감마나이프방사선수술학회 우수발표상 수상
- [동정]원광대학교병원, “퇴원손상심층조사” 로 보건복지부장관상 수상
- [동정]울산대학교병원 이종화 교수, ‘울산의사대상’ 수상
- [인사]경희대병원 장재영 교수, 제14대 대한소화기내시경학회 이사장 선출
- [인사]가천대 길병원 하승연 교수, 대한병리학회 차기 학회장 선출
- [인사]전남대병원 김수완 교수, 대한고혈압학회 제32대 회장 취임
- [부음]박미경 해운대나눔과행복병원 내과부장 부친상
- [동정]서울성모병원 이래석 교수, ‘첨단재생의료 발전 유공’ 보건복지부 장관 표창 수상
- [인사]에스디생명공학, 신임 대표이사에 대원제약 백인영 본부장 선임
- [인사]경희대병원 장재영 교수, 제14대 대한소화기내시경학회 이사장 선출
- [인사]가천대 길병원 하승연 교수, 대한병리학회 차기 학회장 선출
- [인사]전남대병원 김수완 교수, 대한고혈압학회 제32대 회장 취임
- [인사]의료기기협회, ‘2025 KMDIA 보험위원회 정책포럼’ 개최 (11/27)
- [인사]아주대병원 산부인과 김미란 교수, 대한가임력보존학회 회장 선출
- [인사]대한비뇨의학과의사회 문기혁 제16대 회장 당선
- [인사]서울대병원 강형진 교수, 대한혈액학회 차기 이사장 선출
- [인사]광동제약, 경영총괄 사장에 박상영 부사장 승진 발령
- [인사]고대 안암병원 오재령 교수, 한국망막학회 회장 선출
- [동정]한국아스트라제네카 대외협력, 한국보건산업진흥원장 표창 수상
- [동정]충북대학교병원 문형철 박사, 대한감마나이프방사선수술학회 우수발표상 수상
- [동정]원광대학교병원, “퇴원손상심층조사” 로 보건복지부장관상 수상
- [동정]울산대학교병원 이종화 교수, ‘울산의사대상’ 수상
- [동정]서울성모병원 이래석 교수, ‘첨단재생의료 발전 유공’ 보건복지부 장관 표창 수상
- [동정]전남대병원 최인성 교수, 광주 장애인복지 유공 광주시장 표창
- [동정]경희대병원 이승현 교수, 대한폐암학회 국제학술대회서 Best Presentation Award 수상
- [동정]강동경희대학교병원 신원철 교수, 대한신경과학회 ‘JCN 논문상’ 수상
- [동정]울산대병원, ‘재난응급의료 종합훈련대회’ 보건복지부장관 특별상 수상
- [동정]중앙대병원 이다혜·이대용 교수, '두산연강 소아청소년과 학술상’, '보원학술상' 각각 수상













