'79z텔레darknessDB_유흥DB문의|l'검색결과 - 전체기사 중 1,821건의 기사가 검색되었습니다.
상세검색-
티쎈트릭 병용요법, 간세포암 수술 후 보조요법서 무재발 생존율 개선
㈜한국로슈(대표이사 닉 호리지)는 자사 면역항암제 ‘티쎈트릭(성분명: 아테졸리주맙)’과 ‘베바시주맙(제품명: 아바스틴)’의 병용요법이 간세포암 수술 후 보조요법에서 무재발 생존율을 통계적으로 유의하게 개선했다고 18일 밝혔다. 해당 연구 결과는 IMbrave050 3상 연구의 신규 데이터로, 4월 14일부터 4월 19일(현지 시간)까지 미국 올랜도에서 열린 미국암연구학회 연례학술대회(AACR 2023)에서 16일 발표됐다. IMbrave050 임상 연구는 간세포암 진단을 받은 환자 중 외과적 절제술 또는 고주파나 극초단파 등의 소작술을 받은 후 재발 위험이 높은 668명의 환자를 대상으로 한 다기관, 오픈라벨, 무작위 배정 3상 임상 연구다. 연구 결과, 티쎈트릭·베바시주맙(아바스틴) 병용요법은 적극적 관찰군(Active surveillance) 대비 암 재발 위험을 28%(HR 0.72, 95% CI: 0.56-0.93; P=0.0120) 감소시킨 것으로 나타났다. 독립적 검토 시설 평가 무재발 생존율(IRF-RFS) 결과는 임상 하위 그룹 전반에서 대체로 일관되게 나타났다. 주요 2차 평가변수인 전체 생존율은 데이터 분석 시점에서 아직 중앙값에 도달하지
- 노영희 기자
- 2023.04.18 17:01
-

샤페론, 사업개발실 실장에 오연삼 전무 영입
샤페론(대표이사 성승용)이 사업개발실 실장에 오연삼 전무를 영입했다고 13일 밝혔다. 오연삼 전무는 미국 캘리포니아 버클리대학에서 분자세포학을 전공했으며, 노스웨스턴 대학 및 컬럼비아 대학에서 대학원 과정을 마쳤다. 이후 삼성종합기술원, GSK, 한올바이오파마 등에서 사업개발 및 파트너 협상 업무를 담당 했다. 이후 포스코 기술투자에서는 국내외 바이오기업에 다양한 투자를 진행한 경험을 가지고 있다. 샤페론은 오 전무의 다양한 경험과 네트워크를 활용해 국내외 제약바이오 기업을 대상으로 기술이전(L/O) 및 공동 연구개발을 보다 적극적으로 진행해 회사의 성장을 도모할 계획이다. 한편 샤페론은 브릿지바이오테라퓨틱스에 특발성 폐섬유증 치료 후보물질을 기술이전 했으며, 국전약품에는 알츠하이머 치료제 ‘누세린’을 기술이전 했다. 또한 동국제약과는 염증복합체를 이중으로 억제하는 신약 후보물질에 대한 공동연구개발 협약을 체결했으며, 동아ST와는 나노바디 이중항체로 신규타겟 대상 공동연구 개발을 진행하고 있다. 샤페론의 성승용 대표이사는 “오연삼 전무의 영입을 기쁘게 생각한다. 상장하면서 주주들에게 약속한 3년 내에 1조 기술이전이라는 목표에 한걸 더 다가간 느낌이다.”며,
- 메디포뉴스
- 2023.04.13 10:19
-

SK바이오, L하우스 비전 선포식 개최…“글로벌 바이오 허브로 도약”
SK바이오사이언스가 백신 생산공장인 안동 L하우스(이하L하우스)에서 비전 선포식을 열고, ‘One Goal, One Team’을 통해 글로벌 톱-티어(Top-tier) 수준의 역량을 갖춘 ‘글로벌 바이오 허브’로 도약할 것을 다짐했다. SK바이오사이언스는 11일 L하우스에서 안재용 SK바이오사이언스 사장, 김훈 Global R&BD대표, 이상균 L하우스 공장장(부사장) 등 임원진 및 L HOUSE 구성원 450여명이 참석한 가운데 ‘L하우스 비전 선포식’을 개최했다. ‘One Goal, One Team’을 주제로 열린 비전 선포식은 코로나19 팬데믹 기간 L하우스가 달성한 성과와 주요 마일스톤을 함께 돌아보고, 엔데믹 시대로 전환하는 시점에서 향후 미래 전략 및 목표를 공유하는 시간으로 구성됐다. 이상균 L하우스 공장장은 인사말을 통해 “SK바이오사이언스가 지난 3년간 코로나19 팬데믹 기간 팬데믹 대응의 중심에 설 수 있었던 것은 L하우스 구성원들의 값진 노력이 있었기 때문에 가능했다”며 지난 3년간 대한민국의 공중보건 수호를 위해 쉼없이 달려온 L하우스 직원들에게 감사와 격려의 마음을 전했다. 뒤이어 이어진 감사영상에는 대한민국 1호 자체 개발 코
- 노영희 기자
- 2023.04.13 06:43
-

“키트루다, 모든 비소세포폐암 환자의 더 많은 내일을 열어가는 치료 옵션”
한국MSD (임시 대표: 데이빗 조나단 피콕)가 자사의 항 PD-1 면역항암제 ‘키트루다’(성분명: 펨브롤리주맙)의 비소세포폐암 1차 건강보험 급여 확대 1주년을 기념해, 폐암 치료에서 보여준 키트루다의 가치, 혁신과 성과에 대해 조명하는 인포그래픽을 4월 10일 공개했다. ◆키트루다 폐암 1차 급여 1주년, 숫자로 보는 키트루다의 오늘 2022년 3월, 키트루다의 건강보험 급여 적용범위가 ▲PD-L1 발현율이 없는 환자를 포함한 모든 전이성 비소세포폐암 환자 대상 ▲비소세포폐암 1차 고식적 치료 병용 및 단독요법 모두에서 면역항암제 중 최초로 확대되면서 국내 치료 접근성이 크게 향상됐다. 키트루다는 ▲기존 항암화학요법 대비 약 2배 개선된 5년 생존율과 ▲3상 임상 장기 추적관찰 데이터를 통한 치료 효과와 안전성을 확인하면서 명실상부한 전이성 비소세포폐암의 표준 치료 옵션으로 자리매김 했다. 미국종합암네트워크(NCCN, National Comprehensive Cancer Network) 가이드라인은 전이성 비소세포폐암 환자의 글로벌 표준 치료로 키트루다를 가장 높게(Preferred) 권고하고 있다. 한국MSD 항암제사업부 이민희 전무는 “키트루다는 전이
- 노영희 기자
- 2023.04.10 16:04
-

‘R&D에 진심’ 한미, AACR서 새 항암 혁신신약 과제 대거 공개
한미약품이 오는 14일부터 19일까지 미국 플로리다주 올랜도에서 열리는 미국암연구학회(AACR 2023)에서 대폭 확대된 항암 분야 혁신신약 파이프라인을 대거 공개한다. 한미약품은 이번 AACR에서 ▲LAPSIL-2 analog(HM16390) 2건 ▲EZH1/2 이중저해제(HM97662) ▲SOS1 저해제(HM99462) ▲YAP/TAZ-TEAD 저해제 ▲mRNA 항암백신 등에 관한 연구결과와 북경한미약품이 주도적으로 개발하고 있는 이중항체 플랫폼(펜탐바디) 기반의 ▲PD-L1/4-1BB BsAb(BH3120) 1건 등 총 7건의 연구결과를 포스터로 발표한다고 5일 밝혔다. IL-2는 세포독성림프구를 분화/활성화하는 물질로, 현재 승인된 재조합 인간 IL-2 (aldesleukin)는 충분한 항종양 효능을 위해 고용량을 사용할 때 혈관누출증후군 등 심각한 부작용이 수반돼 사용에 제한이 있다. 한미약품이 개발중인 HM16390은 IL-2 수용체들 간의 결합력을 최적화해 강력한 항종양 효능은 물론 안전성까지 개선한 후보물질이다. 항암 주기당 1회 피하 투여가 가능한 제형으로 현재 임상 1상 진입을 위한 독성 연구가 진행되고 있다. 이와 함께 한미약품은 EZH1
- 노영희 기자
- 2023.04.05 10:51
-
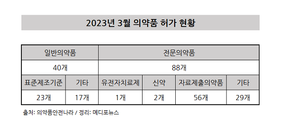
3월 허가된 의약품은 총 128건…전문의약품 68.7%
2022년 3월 식품의약품안전처로부터 품목허가를 받은 의약품이 총 128건으로 확인된 가운데, 이 중 전문의약품은 약 68.7%의 비중인 88개로 확인됐다. 3월에 허가된 전문의약품 중에서는 유전자치료제 1개와 신약 2개 품목이 포함돼있는데 이 중 유전자치료제는 한국얀센의 ‘카빅티주’가 포함됐다. 카빅티주는 CAR-T 치료제로, 환자의 T세포에 B세포 성숙항원을 인지할 수 있는 유전정보를 넣어 이를 환자의 몸에 주입하는 원리의 항암제다. 해당 적응증은 다발골수종으로 프로테아좀억제제, 면역조절제제, 항-CD38 항체를 포함해 적어도 4가지 치료를 받은 재발 또는 불응성 환자에게 사용된다. 카빅티주의 주요 특징으로는 첨당재생바이오법(첨생법)에 따라 ‘장기추적조사’ 대상이 된다는 것으로, 투여일로부터 15년 동안 이상사례 현황을 추적조사해야 하는 약품이다. 기타 자료제출의약품 중에서는 희귀의약품에 속하는 폼페병 치료제인 사노피의 ‘넥스비아자임(성분명 아발글루코시다제 알파)’가 장기 효소 대체 요법으로 허가를 받았다. 특히 희귀의약품 중에서는 최초의 개량생물 의약품으로 허가됐다. 폼페병은 근육 속 글리코겐 분해 효소인 ‘산성 알파 글루코시다제’의 결핍으로 발병하는
- 노영희 기자
- 2023.04.05 05:32
-

Tianlong, 신제품 2종 글로벌 출시 발표
-- GeneFlex 핵산 추출기와 Gentier mini+ 실시간 PCR 시스템 -- 유연성 및 휴대성 선보이며, 소규모 실험실이나 현장 테스트 수요에 이상적 (시안, 중국 2023년 4월 3일 PRNewswire=모던뉴스) 분자 진단 제품을 전문으로 하는 혁신적인 첨단 기술 기업인 Tianlong[ https://www.medtl.net/ ]이 GeneFlex 핵산 추출기(GeneFlex Nucleic Acid Extractor)와 Gentier mini+ 실시간 PCR 시스템(Gentier mini+ Real-time PCR System)의 신제품 2종을 글로벌 출시한다고 발표했다. 소형 디자인과 휴대성을 특징으로 하는 이들 두 제품은 연구원과 임상의에게 핵산 추출과 실시간 PCR 적용을 위한 효율적이고 신뢰성 높은 도구를 제공할 수 있다. Tianlong의 CEO Li Ming은 "수많은 실험실과 임상 업체가 공통으로 고민하는 2가지 사항은 처리량의 낭비와 공간&nbs
- PR Newswire
- 2023.04.03 12:54
-
‘’옵디보-여보이’ 병용 및 ‘옵디보-화학요법 병용’ 적응증 추가
한국오노약품공업(대표이사: 최호진)과 한국BMS제약(대표이사: 이혜영)은 3월 22일 항 PD-1 단일클론항체인 옵디보(성분명: 니볼루맙)가 식품의약품안전처로부터 PD-L1 발현 양성(≥1%)으로서 절제불가능한 진행성 또는 전이성 식도 편평세포암(ESCC)의 1차 치료로서 하기 2가지 병용요법에 대한 적응증을 추가 승인 받았다고 밝혔다. 해당 적응증은 △옵디보-여보이(성분명: 이필리무맙) 병용요법 △옵디보-플루오로피리미딘계 및 백금 기반 화학요법 병용요법이다. 이번 승인은 이전 치료 경험이 없는 절제 불가능한 진행성, 재발성 혹은 전이성의 식도 편평세포암 환자를 대상으로 옵디보-여보이 병용 및 옵디보-화학요법 병용을 화학요법 단독과 비교 평가한 다기관, 글로벌, 무작위배정, 오픈라벨 3상 임상 CheckMate-648(ONO-4538-50/CA209648) 결과를 기반으로 이뤄졌다. 해당 임상 결과, 사전 지정된 중간 분석에서 옵디보를 사용한 2가지 병용요법은 화학요법 단독 대비 PD-L1 발현율이 1% 이상인 환자군 및 무작위 배정된 전체 환자군을 대상으로 통계적으로 유의하고 임상적으로 의미있는 전체생존기간(OS) 개선을 보여줬다. 해당 임상시험에서 옵디보
- 노영희 기자
- 2023.03.27 11:06
-
판시딜, ‘한국산업의 브랜드파워’ 탈모치료제 부문 5년 연속 1위
약용효모 성분의 탈모 치료제인 동국제약(대표이사 송준호) 판시딜이 한국능률협회컨설팅이 발표한 ‘2023년도 제25차 한국산업의 브랜드파워’ 조사결과에서, 소비재 산업군 ‘탈모치료제’ 부문 5년 연속 1위에 선정되며 브랜드 가치를 입증 받았다. ‘한국산업의 브랜드파워(K-BPI)’는 대한민국 소비생활을 대표하는 각 산업의 제품 및 서비스, 기업의 브랜드 경쟁력을 측정하는 지수로, 한국능률협회컨설팅(KMAC)이 1999년 국내 최초로 개발한 브랜드 평가 모델이다. 전국 1만 2300명의 소비자를 대상으로 일대일 면접 조사를 거쳐 산업 부문별 대표 브랜드를 선정한다. ‘판시딜’은 전년보다 5% 상승한 브랜드파워 지수(K-BPI) 787.9점(1,000점 만점 중)을 획득했으며, 2위 브랜드와는 380점의 격차를 보이며 압도적인 1위를 차지했다. 브랜드 인지도와 브랜드 충성도 항목 모두 높은 점수로 우위를 나타냈다. 특히, 최초 인지도가 73.4%로 전년 대비 24%나 상승해 2위, 3위 브랜드와 큰 차이를 보였다. K-BPI 세부 항목별 최고 점수를 받은 것은 판시딜이 일반의약품 경구용 탈모치료제 중 9년 연속 판매 1위(2014년~2022년 IQVIA 데이터 기
- 노영희 기자
- 2023.03.24 16:09
-

테라펙스, 4세대 비소세포폐암 치료제 후보물질 임상자문위원회 개최
㈜테라펙스(대표 이구)는 4세대 비소세포폐암 치료제(EGFR 저해제) 후보물질인 ‘TRX-221’의 제 1차 임상자문위원회를 22일 인터콘티넨탈 호텔에서 개최했다고 23일 밝혔다. 임상자문위원회는 임상승인 신청을 앞두고 임상설계를 협의하는 회의체다. 이날 임상자문위원회에는 국내의 저명한 폐암 전문 임상의인 ▲서울아산병원 김상위 교수, 이대호 교수, ▲연세암병원 조병철 교수, 임선민 교수, ▲삼성서울병원 안진석 교수, ▲충북대학교병원 이기형 교수 등이 참석, ‘TRX-221’ 개발전략에 대한 심도 깊은 논의가 이뤄졌다. ‘TRX-221’은 비소세포폐암 치료제로 널리 쓰이는 타그리소(성분명 오시머티닙) 등 3세대 EGFR 저해제 치료 이후 나타나는 내성 돌연변이인 C797S 뿐만 아니라 1, 2, 3세대 EGFR 저해제가 타겟하는 돌연변이(Del19, L858R, T790M 등)까지 저해하는 광범위 4세대 EGFR 저해제(broad spectrum 4th Gen EGFR TKI) 후보물질이다. 이날 임상자문위원회에 참석한 자문위원들은 ‘C797S’ 변이 동물모델에서뿐만 아니라 다양한 EGFR 돌연변이 종양모델에서 1일 1회 경구투약으로 체중감소 없이 용량의존적
- 노영희 기자
- 2023.03.24 08:30
-

순천향대 천안병원 양은정 교수, ‘생애 첫 연구과제’ 선정
순천향대학교 부속 천안병원 산부인과 양은정 교수가 최근 정부가 시행한 ‘2023년도 상반기 기초연구사업-생애 첫 연구 과제’에 선정됐다. 과학기술정보통신부와 한국연구재단이 지원하는 사업은 우수한 신진 연구자를 발굴하고, 과학기술 미래역량을 확충하기 위해 만 39세 이하 연구자를 대상으로 매년 진행된다. 양 교수의 선정과제는 ‘자궁경부암에서 PD-L1과 관련된 종양 대식 세포의 CCL2-CCR2의 탐색 및 제어를 통한 면역치료 방법 제시(Proposal of immunotherapy method through search and control of CCL2-CCR2 of tumor associated macrophages with PD-L1 in cervical cancer)로 3년간 1억원의 연구비를 지원 받는다. 양은정 교수는 “자궁경부암 환자들의 면역항암제 치료 반응성을 증가시키는 기술을 제시하고 지금보다 더 효과적인 새로운 치료법을 모색할 계획”이라며, “자궁경부암 환자 치료와 생존율 향상에 도움이 되도록 최선을 다하겠다”라고 말했다.
- 메디포뉴스
- 2023.03.23 14:09
-

AMGEN과 NSG BIOLABS, 제1회 AMGEN GOLDEN TICKET 우승자 발표
-- 제1회 우승 기업은 'ALBATROZ THERAPEUTICS'-- Golden Ticket, 생명공학 스타트업의 역량을 촉진하고, 동남아시아의 새로운 생명공학 에코시스템을 더욱 발전시키는 데 일조할 전망 (싱가포르 2023년 3월 20일 PRNewswire=모던뉴스) 세계 선도적인 생명공학 기업 Amgen과 싱가포르 최대 규모의 생명공학(바이오테크) 공동 작업 실험실 및 사무실 공급업체인 NSG BioLabs가 Albatroz Therapeutics를 제1회 싱가포르 Amgen Golden Ticket 우승자로 발표했다. Albatroz Therapeutics는 모든 장비를 갖추고 인증을 받은 NSG Biolabs 턴키 BSL-2 실험실 1년 무료 이용권을 비롯해
- PR Newswire
- 2023.03.20 11:00
-

써모 피셔 사이언티픽, 싱가포르 협력 센터 통해
아태지역 세포 치료 연구 지원 프로그램 실시 - 아시아태평양 전역의 세포 유전자 치료 개발을 가속화하기 위해 싱가포르에서 프로그램 시행 - 프로그램을 통해 차세대 생명을 구하기 위해 약물 및 치료제를 개발하는 연구자들이 환자 결과를 더욱 개선할 수 있도록 모든 단계의 여정을 지원할 것 (서울, 대한민국 2023년 3월 20일 PRNewswire=모던뉴스) 세계적인 과학 기업 써모 피셔 사이언티픽(Thermo Fisher Scientific Inc. 이하 써모 피셔)은 아시아태평양 지역에 걸쳐 세포 치료 개발을 가속화하기 위해 싱가포르에 새로운 세포 치료 협력 센터&nb
- PR Newswire
- 2023.03.20 10:30
-

“K-뷰티 강자 수식…오리지널리티가 비결입니다”
‘울트라브이(UltraV)’는 국내 녹는실 브랜드로 가장 잘 알려진 기업 중 하나로 녹는실 리프팅 열풍의 시초이기도 하다. 현재는 약 50여개국에 진출한 세계적인 브랜드로 성장했으며, 그 바탕에는 권한진 대표의 피땀 어린 노력이 있다. 일주일 중 3일은 병원 진료를, 또3일은 해외에서 세미나를 하고,하루는 비행기 안에서 시간을 보낼 만큼 권한진 대표의 시간은 바쁘게 흘러간다. 울트라브이를 글로벌한 기업으로 성장시키며‘K-뷰티의 강자’로 떠오른 권한진 대표의 이야기를 들어봤다. Q. 울트라브이에 대한 소개 부탁드립니다. A. 울트라브이 대표이사이자 전 세계 16개 네트워크를 운영하는 더마스터의원 네트워크의 대표원장 권한진입니다. 저희 울트라브이는 2012년도에 설립된 녹는실 리프팅, 화장품, 의료기기 등을 생산하고 판매하는 회사입니다. Q.포트폴리오를 확장하며울트라브이를 글로벌한 회사로 성장시키셨습니다. 과정을 설명해주시자면? A. ‘K-미용의료’라는 얘기가 있는데, 잘 살펴보면 한국에 오리지널리티(Originality)가 있는 제품은 거의 없습니다. 보툴리눔 톡신이나 필러 등 한국에서 시작해서 퍼져나간 것이 없다는 뜻입니다. 한국에 오리지널리티가 있는 거의
- 이윤희 기자
- 2023.03.18 06:00
-

Sai Life Sciences, 맨체스터 Alderley Park에 GMP Kilo Lab 설립
잉글랜드 맨체스터 및 인도 하이데라바드, 2023년 3월 16일 /PRNewswire/ -- 세계 선도적인 의약품 위탁연구 및 위탁개발생산 기업(CRO-CDMO)[https://www.sailife.com/?utm_source=pr&utm_medium=web&utm_campaign=manchester-kilolab ]인 Sai Life Sciences가 영국 맨체스터 Alderley Park에 위치한 시설에 GMP Kilo Lab을 설립한다고 발표했다. Sai Life Sciences는 고객 임상 요건을 빠르게 충족하기 위해 새로운 GMP Kilo Lab을 통해 그램 단위에서 킬로그램 단위로 원료 의약품과 약제 중간물을 공급할 예정이다. Sai Life Sciences sets up GMP Kilo Lab in Alderley Park, Manchester, UK Sai Life Sciences의 COO Sauri Gudlavalleti는 이번 발표를 통해 "고객과 더 가까워진 신규 실험실은 포괄적인 cGMP 관리와 세계적 수준의 인프라를 갖춘 곳"이
- PR Newswire
- 2023.03.16 19:22
-

휴젤, ‘2023 포커스 그룹 세미나’ 개최
글로벌 토탈 메디컬 에스테틱 전문 기업 휴젤㈜(대표집행임원 손지훈)이 오는 18일 대전 호텔오노마에서 ‘2023 휴젤 포커스 그룹 세미나’를 개최한다고 16일 밝혔다. 포커스 그룹 세미나는 최신 시술 기법 및 트렌드 교육에 대한 HCPs(의료 전문가)의 높은 수요에 맞춰 마련된 지역별 학술 행사로, 지난해 인천을 시작으로 부산ㆍ서울까지 총 3개 도시에서 강연을 진행, 회차별 참여 만족도가 90% 이상을 기록하며 성황리에 마무리된 바 있다. 올해 세미나는 ‘엔데믹 시대, 필터나 보정 없이 자신만의 아름다움을 찾는다’는 의미에서 ‘Turn off the filter, and find your beauty persona’를 주제로 대전, 부산, 서울에서 순차적으로 진행된다. 첫 개최지인 대전에서는 올해 2월 남녀 소비자 700명을 대상으로 진행한 뷰티 트렌드 조사 결과를 발표, 2040 남녀 소비자들이 선호하는 얼굴 부위별 ‘뷰티 페르소나(Beauty persona Trend)’가 공개된다. 이어 아카데미 세션에서는 보툴리눔 톡신ᆞHA 필러 및 스킨부스터ᆞ리프팅 실 시술과 임상 사례 강연이 진행된다. 황승국 원장(세븐데이즈 성형외과)의 ‘더모톡신(Dermotoxi
- 이윤희 기자
- 2023.03.16 13:11
-

보령, ‘핀쥬베스프레이’
보령(대표 장두현)이 국내 최초 스프레이 제형 피나스테리드 탈모약인 ‘핀쥬베스프레이 (Finjuve Spray) 2.275mg/mL’를 오는 21일 출시할 예정이다. 보령은 지난해 1월, 알미랄로부터 핀쥬베스프레이 국내 독점 판권을 확보한 이후, 같은 해 9월 품목허가를 거쳐 올해 3월 21일 국내 최초로 정식 출시하게 됐다. 핀쥬베스프레이는 피부과 의약품 전문 글로벌 제약사인 알미랄(Almirall, S.A.)에서 개발한 탈모치료제로, 성인 남성의 안드로겐성 탈모증에 처방되는 피나스테리드 성분을 경구용이 아닌 스프레이 제형으로 개발한 제품이다. 탈모 부위 두피에 직접 분무되는 국소 치료 방식으로, 경구용 피나스테리드에 비해 혈중 농도를 낮춰 부작용이 감소한 것이 가장 큰 장점이다. 반면, 치료 효과는 경구용 피나스테리드와 동등한 수준이다. 3상 임상시험 결과, 투여 24주 후 경구용 피나스테리드 1mg 대비 타겟 부위의 모발 수(TAHC, Target Area Hair Count)에서 동등한 수준의 효과를 확인 반면, 혈중 농도는 100분의 1 수준을 보이며, 투여 후 발생한 이상사례 발생률이 경구 피나스테리드 투여군보다 낮았다. 또한 핀쥬베스프레이는 피부
- 보령
- 2023.03.13 10:31
-

샤페론, ‘2023 바이오-유럽 스프링 컨퍼런스’ 참가
샤페론(대표이사 성승용)은 오는 3월 20일부터 22일까지 ‘바이오 유럽 스프링(BIO-Europe Spring)’에 참가한다고 13일 밝혔다. ‘바이오-유럽 스프링’은 세계 제약·바이오 기업 및 관련 투자자들이 참석해 다양한 기술제휴와 연구협력, 투자유치를 논의하는 유럽 최대 규모의 바이오 컨퍼런스다. 오는 20일(현지시간)부터 22일까지 스위스 바젤에서 진행되며, 올해는 ‘노바티스’, ‘사노피’, ‘MSD’ 등 글로벌 제약·바이오기업이 대거 참석한다. 특히, 이번 행사에서 샤페론은 기업 프레젠테이션(Company Presentation)사에 선정되며 기술에 대한 잠재력을 인정받았다고 회사측은 밝혔다. 샤페론은 이번 발표에서 자사의 핵심 기술과 주력 파이프라인 개발 현황에 대해 소개할 계획이다. 이와 더불어, 임상 결과를 기반으로 글로벌 제약·바이오 기업들과 파트너십 미팅을 통해 글로벌 기술이전 등 전략적 파트너십 발굴에 박차를 가할 예정이다. 샤페론은 독자적인 염증복합체 억제제 기술을 기반으로 아토피 피부염 치료제 ‘누겔(NuGel)’과 코로나19 치료제 ‘누세핀(NuSepin)’, 알츠하이머 치매 치료제 ‘누세린(NuCerin)’을 개발하고 있다. 회사
- 노영희 기자
- 2023.03.13 10:17
-

온코닉테라퓨틱스 P-CAB 신약, 中에 1600억원 규모 기술수출
온코닉테라퓨틱스가 개발 중인 위식도 역류질환 치료 신약이 중국 제약사에 기술수출됐다. 온코닉테라퓨틱스(대표 김존/이하 온코닉)는 중국 상장 제약사인 리브존파마슈티컬그룹(이하 리브존)과 위식도 역류질환 치료제 ‘자스타프라잔(Zastaprazan, 개발코드명 JP-1366)’의 개발 및 상업화에 대해 총 1억 2750만달러(한화 약 1600억원) 규모의 기술수출 계약을 체결했다고 10일 밝혔다. 이번 기술수출에 따라 온코닉은 반환의무가 없는 계약금 1500만달러(약 200억원)를 우선 지급받게 된다. 이와 함께 개발과 허가, 상업화 단계별 마일스톤(milestone)으로 최대 1억 1250만 달러(약 1450억원)의 기술료를 받을 수 있게 됐다. 계약금 및 마일스톤 단계별 금액의 수취 후 반환의무는 없으며, 상업화 이후 매출에 따른 로열티를 추가로 지급받게 된다. 중국 광둥성(廣東省) 주하이(珠海)시에 본사를 두고 있는 리브존은 연구개발부터 제조 및 판매에 이르는 종합 제약기업이다. 2021년 기준 중국 내 매출액 18억 8000만 달러(약 2.4조원)를 기록했으며 위식도 역류질환 분야에서 연간 4억 5000만달러(약 6천억원) 이상의 매출을 올리고 있다. 현재
- 노영희 기자
- 2023.03.10 15:10
-

이수앱지스, 알츠하이머 신약 기술이전 가능성 타진
이수앱지스가 사업화를 추진중인 알츠하이머 신약 후보물질(ISU203)의 동물실험 내용이 세계적인 신경계 질환 학회들의 주목을 받고 있다. 이수앱지스는 알츠하이머 질환 동물 모델 실험에서 ISU203이 신경염증을 감소시켜 인지기능 손상을 개선시킨다는 결과를 확인했다. 이 같은 실험결과는 생명공학분야의 세계적 학회인 키스톤 심포지아(Keystone Symposia)와 신경질환학회(Neurological Disorders Summit)에서 공개된다. 이번 글로벌 학회 발표를 통해 이수앱지스는 ISU203의 혁신신약(First-in-Class) 가능성을 해외에 알리고 기술수출 가능성을 타진한다는 계획이다. 이번 키스톤 심포지아는 오는 5월, 5일 동안 캐나다 휘슬러에서 개최되며 신경염증 및 신경질환을 주제로 한다. 특히 대표 강연자로 선정된 버지니아 만이 리(Virginia Man-Yee Lee) 교수는 신경퇴행성 질환 연구로 지난해 노벨생리의학상 후보에 오른 신경질환분야 권위자로 이번 학회에 대한 세계적인 관심이 집중돼 있다. 오는 6월에는 이탈리아 로마에서 개최되는 신경질환학회(Neurological Disorders Summit)에 ISU203의 포스터 발표가
- 노영희 기자
- 2023.03.09 20:14
- [부음]이혁 한국임상고혈압학회 회장 모친상
- [화촉]박희용 前 중앙약대 교수·김미경 前 베링거인겔하임 전무 차남 (9/7)
- [부음]안지선 헤일리온코리아 본부장 부친상
- [부음]현수환 동원약품 회장 별세
- [부음]조준 강릉 조소아과의원 원장 · 조승주 조선대 의대 교수 모친상
- [인사]질병관리청 공무원 인사발령 (8/1)
- [동정]국립암센터 김열 교수, 대한금연학회 회장 취임
- [동정]강동경희대학교한방병원 박성욱 교수, 과학기술 우수논문상 수상
- [화촉]호필수 샤페론 전무 아들 (8/9)
- [동정]한림대성심병원 노규철 교수, 국제학술지 ‘최다 열람 논문’ 선정
- [인사]질병관리청 공무원 인사발령 (8/1)
- [인사]GSK 한국법인 구나 리디거 신임 대표이사 취임 (8/1)
- [인사]보건복지부 인사 발령 (7/22)
- [인사]아주대병원 장석준 교수, 아시아부인종양학회 회장 취임
- [인사]시밀러 전문가 홍승서박사, 대웅제약 BS사업본부장으로 선임
- [인사]한국아스텔라스 이선희 전무, 아스텔라스 이집트 사장 영전 (8/1)
- [인사]을지재단 2025년 정기인사
- [인사]한국팜비오, 중외제약 출신 영업 임원 2명 영입
- [인사]질병관리청 임승관 신임청장 취임 (7/14)
- [인사]로슈진단 신임 분자진단 사업본부장 조승희 전무 선임
- [동정]국립암센터 김열 교수, 대한금연학회 회장 취임
- [동정]강동경희대학교한방병원 박성욱 교수, 과학기술 우수논문상 수상
- [동정]한림대성심병원 노규철 교수, 국제학술지 ‘최다 열람 논문’ 선정
- [동정]서울의대 묵인희 교수, 美 알츠하이머협회 국제학술대회(AAIC)서 기조강연
- [동정]서영석 의원, ‘2025 대한민국 헌정대상’ 수상
- [동정]고려의대 안형진 교수, 복지부 장관 표창 수상
- [동정]순천향대 부천병원 신희준 교수 ‘대테러의학’, 대한민국학술원 우수학술도서 선정
- [동정]단국대병원 노상철 교수팀, ‘과학기술우수논문상’ 수상
- [동정]울산대학교병원 이현준·박기봉 교수, 골반 골절 수술 성과 SCIE 국제학술지 발표
- [동정]한림대강남성심병원 김혜원 교수, 보건의료 R&D 우수성과 30선 선정
- [화촉]박희용 前 중앙약대 교수·김미경 前 베링거인겔하임 전무 차남 (9/7)
- [화촉]호필수 샤페론 전무 아들 (8/9)
- [화촉]정영기 대한약사회 대외협력본부장 장녀 (9/14)
- [화촉]김성원 대림성모병원 이사장 장남 (8/30)
- [화촉]김현경 한국오가논 대외협력부 차장 (8/23)
- [화촉]유철진 조선약대 수도권동문회 부회장 딸 (7/26)
- [화촉]신명수 안성시약사회장 딸 (7/13)
- [화촉]유철진 조선약대 수도권동문회 부회장 딸 (7/26)
- [화촉]양영은 제주지오영 대표 장녀 (7/5)
- [화촉]조헌제 한국신약개발연구조합 전무이사 장남 (8/9)










