-
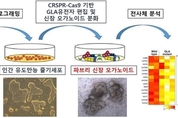
신장 오가노이드 이용한 ‘난치성 파브리 신장병’ 치료제 개발
난치성 유전 질환인 파브리 신장병의 치료제 개발이 성공하면서 새로운 희망의 길이 열리게 됐다. 가톨릭대학교 성빈센트병원 신장내과 김용균 교수팀(가톨릭대학교 의과대학 세포사멸질환 연구센터, (주)알젠오가노 바이오테크놀로지)이 인간 유도 만능 줄기세포로 만든 ‘미니 신장’ 신장 오가노이드를 이용해 난치성 유전질환인 파브리 신장병을 모사(模寫)해 발병 원인을 규명하고 치료제 개발에 성공했다. 특히, 이번 연구는 차세대 신약 개발 및 재생 치료의 핵심 요소 중 하나로 꼽히는 ‘신장 오가노이드’를 연구에 이용했다는 점에서 더욱 높은 평가를 받고 있다. 신장 오가노이드는 줄기세포에서 분화되며 실제 인간의 신장을 구성하는 세포들로 이뤄져 있어 인간 신장과 구조 및 기능이 매우 유사한 3차원 세포 구조체로, ‘미니 신장’이라고도 불린다. 김용균 교수팀이 치료제 개발에 성공한 ‘파브리 신장병’은 우리 몸에 갈락토시데이즈-알파(galactosidase alpha)라는 특정 효소가 부족해 생기는 희귀 유전 질환인 파브리병이 신장에 침범하는 것으로, 말기 신부전으로 진행해 투석치료 또는 신장 이식이 필요한 위험한 질환이다. 파브리병의 치료는 α-Gal A 효소를 주입하는 ‘효소
- 신대현 기자
- 2021-11-16 13:51
-

신장 세뇨관-혈관 관상 구조체, 3D 바이오프린팅 성공
포항공대 조동우 교수와 가톨릭대학교 성빈센트병원 신장내과 김용균 교수팀이 3D 바이오 프린팅 기술로 신장에서도 고난도로 꼽히는 근위 세뇨관과 혈관이 결합된 관상 구조체를 만드는데 성공했다. 인간의 신장은 모세혈관 덩어리인 사구체와 보먼주머니, 세뇨관이 연결된 네프론이라는 조직으로 구성되어 있는데, 사구체에서 여과된 모세혈관 내 노폐물은 세뇨관을 지나며 재흡수와 분비 과정을 거쳐 최종적으로 소변으로 배출되게 된다. 이때 세뇨관은 세뇨관을 둘러싼 혈관과 지속적인 상호 작용을 하며, 사구체에서 여과된 필수적인 물질들을 재흡수하고, 독성 물질 등은 밖으로 내보내는 기능을 한다. 조동우·김용균 교수팀이 성공한 3D 신장 세뇨관-혈관 관상 구조체는 실제 인간의 신장처럼 미세 혈류가 흐를 수 있고 신장의 필수 기능인 근위 세뇨관과 혈관 사이의 재흡수 및 분비 기능을 정밀하게 구현했다. 또한 이 구조체를 실험용 쥐의 신장에 이식했을 때 성공적으로 생착 되었으며, 신장 질환이 있는 실험용 쥐에 이식했을 때 질환 일부가 호전되는 모습을 확인했다. 3D 신장 세뇨관-혈관 관상 구조체는 기존의 비용과 시간이 많이 드는 동물 실험을 대체해 시험관 내에서 신장 약물 독성 실험, 신장
- 신대현 기자
- 2020-10-26 11:14
- [인사]대원제약 정기 승진 인사 (3/1)
- [동정]여의도성모병원 윤혜연 교수, 한국각막학회 국제학술대회 ‘Best Presentation Award’ 수상
- [동정]고대구로병원 이승룡 교수, '제19회 암 예방의날' 행사서 ‘국무총리 표창’ 수상
- [인사]CSL, 한국 법인에 황세은 신임 대표 선임
- [동정]부천성모병원 지희정 간호사, ‘암 예방의 날’ 보건복지부 장관 표창 수상
- [동정]휴온스, 성남상공대상서 ‘ESG경영대상’ 수상
- [동정]김상진 대한가정의학과의사회 의무이사, 보건복지부 장관표창 수상
- [동정]고대 안산병원 민경진 교수, ‘제19회 암 예방의 날 기념식’ 보건복지부장관 표창
- [동정]충남대학교병원 박수용 교수, 대한진단혈액학회 학술대회 최우수 구연상
- [동정]제19회 암예방의 날, 국립암센터 이건국 연구소장 ‘국민포장’, 최정미 사무국장 ‘국무총리 표창’ 수상
- [인사]대원제약 정기 승진 인사 (3/1)
- [인사]CSL, 한국 법인에 황세은 신임 대표 선임
- [인사]충북대병원 최미영 교수, 제18대 한국사시소아안과학회 회장 선출
- [인사]질병관리청 공무원 과장급 전보 (3/16)
- [인사]식약처 국·과장급 인사발령 (3/16)
- [인사]강동경희대학교병원 김동환 교수, 대한암재활학회 차기 회장 선출
- [인사]경희대학교병원 백종우 교수, 한국자살예방협회 회장 취임
- [인사]단국대병원 박재석 교수, 대한결핵 및 호흡기학회 회장 취임
- [인사]원텍, 영업총괄·권역별 법인장·연구소장 인사 단행
- [인사]질병관리청 승진 및 전보 (3/9)
- [동정]여의도성모병원 윤혜연 교수, 한국각막학회 국제학술대회 ‘Best Presentation Award’ 수상
- [동정]고대구로병원 이승룡 교수, '제19회 암 예방의날' 행사서 ‘국무총리 표창’ 수상
- [동정]부천성모병원 지희정 간호사, ‘암 예방의 날’ 보건복지부 장관 표창 수상
- [동정]휴온스, 성남상공대상서 ‘ESG경영대상’ 수상
- [동정]김상진 대한가정의학과의사회 의무이사, 보건복지부 장관표창 수상
- [동정]고대 안산병원 민경진 교수, ‘제19회 암 예방의 날 기념식’ 보건복지부장관 표창
- [동정]충남대학교병원 박수용 교수, 대한진단혈액학회 학술대회 최우수 구연상
- [동정]제19회 암예방의 날, 국립암센터 이건국 연구소장 ‘국민포장’, 최정미 사무국장 ‘국무총리 표창’ 수상
- [동정]가천대 길병원 이기택 교수, 암예방의 날 대통령 표창
- [동정]제주대학교병원 홍지수 간호사, ‘제6회 미래선도 간호사상’ 수상













