[비뇨기∙기타암 편] 2019년 FDA 허가로 살펴본 항암분야 성과
비뇨기암서 키트루다 콤보∙Balversa∙엑스탄디 등의 옵션 등장
흑색종 및 자궁내막암에 키트루다 연이은 허가
- 양민후 기자 minhuy@medifonews.com
- 등록 2020-01-14 05:50:00
항암분야는 지난해 반가운 소식으로 가득했다. 소화기암(간암·식도암·췌장암), 폐암, 혈액암 그리고 유방암 등에 새로운 무기를 제시하며 경과
향상을 이끌었다. 성과는 미국식품의약국(FDA)의 허가 사항에서
확인할 수 있었다. FDA가 2019년 주요 암종 치료에
대해 내린 결정을 3편에 걸쳐 되짚어본다. [편집자 주]
비뇨기계에선 신장암∙방광암∙전립선암 등에 대한 치료옵션이 등장했다. ‘키트루다(성분명:펨브롤리주맙, 제약사:MSD)’는 ‘인라이타(엑시티닙, 화이자)’와 짝을 이뤄 신세포암 치료의 표준을 정립했다. 신규기전 약물 ‘Balversa(erdafitinib, 얀센)’는 방광암 치료에 대안을 제시했다. 흑색종 및 자궁내막암 등
기타암에서는 키트루다가 연이어 효과를 입증했다. 키트루다는 흑색종에서 수술후보조요법에 허가됐고, 자궁내막암에선 ‘렌비마(렌바티닙, 에자이)’와의 병용요법이 승인됐다.
◇ 신세포암에 키트루다 콤보
표준..방광암에 FGFR억제기전 Balversa 등장
신세포암에
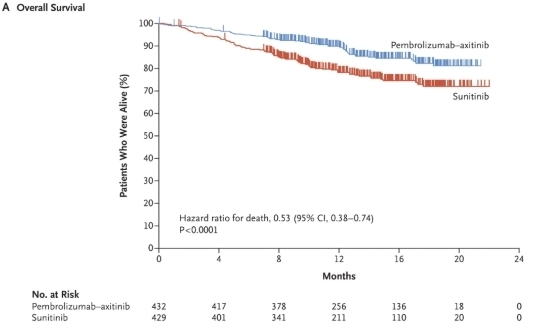
대해선 면역항암제∙혈관내피세포성장인자(VEGF) 억제제 조합이 표준으로 등극했다. 키트루다∙인라이타 병용요법의 효능은 KEYNOTE-426(3상)에서 나타났다. 연구는 신규 진행성 신세포암 환자들을 대상으로 실시됐다. 대조약은 수텐(수니티닙, 화이자)이었다. 연구결과, 키트루다∙인라이타
콤보군은 대조군에 견줘 사망위험이 47% 감소한 것으로 조사됐다[위험비(HR):0.53]. 무진행생존기간(PFS) 중앙값은 키트루다 콤보군
15.1개월, 대조군 11.1개월이었다(HR:0.69). 이 결과를 바탕으로 키트루다∙인라이타 콤보는 진행성 신세포암
1차치료에 허가됐다.
MSD 소속 Monaco 박사는 “키트루다∙인라이타 콤보는 KEYNOTE-426에서 표준치료보다 우수한 전체생존기간(OS) 및 PFS 등을 기록했다”며 “콤보의 효능은 환자의 특성과 관계없이 일정하게 나타났다”고 정리했다.
전이성 방광암에 대해선 FGFR 억제기전신약 Balversa가 대안으로 등장했다. 허가는 2상(단일군) 연구결과를 바탕으로 한다. 연구에는 백금기반 항암화학요법 경험이 있는 FGFR3/FGFR2 변이 전이성 방광암 환자들이 참여했다. Balversa는 해당 환자군을 대상으로 객관적반응률(ORR) 32%[완전반응(CR):2.3%]라는 성적을 남겼다.
전립선암에는
‘엑스탄디(엔잘루타마이드,
아스텔라스)’가 활로를 제시했다. 엑스탄디는
ARCHES(3상) 결과에 근거, 거세민감성 전립선암 적응증을
획득했다. 구체적으로 엑스탄디∙안드로겐 차단요법(ADT)은
위약∙ADT 치료 대비 질환진행 및 사망위험을 약 61% 줄였다.
◇ 흑색종∙자궁내막암서 키트루다 잇따른 허가
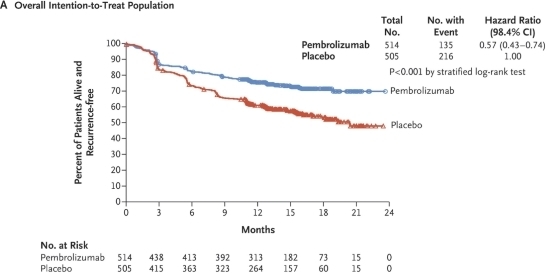
흑색종에선 키트루다가 수술후보조요법으로 활용도를 넓혔다. 적응증 확대는 EORTC 1325/KEYNOTE-054(3상) 결과에 기반했다. 연구는 3기 고위험 흑색종 환자들을 대상으로 시행됐다. 참여자들은 완전절제술을 경험했다. 연구결과, 무재발생존기간(RFS) 중앙값은 위약군 20.4개월이었다. 키트루다군은 중앙값에 도달하지 않았다. 이는 키트루다군이 위약군 대비 재발∙사망 위험이 43% 감소한 것으로 풀이된다(HR:0.57). 키트루다의 효능은 PD-L1 발현률 및 BRAF 변이 여부와 무관하게 일정했다.
자궁내막암 치료분야에서도 면역항암제∙VEGF억제제 조합의 허가사례를 확인할 수 있었다. 키트루다와 렌비마 병합요법은 반응률을 바탕으로 진행성 자궁내막암 후속치료에 승인됐다. Study111/KEYNOTE-146(2상∙단일군) 결과가 근거를 제공했다. 연구에는 치료를 경험한 자궁내막암 환자들이 참여했다. 키트루다∙렌비마 콤보는 참여자 중 현미부수체불안정(MSI-H)/불일치복구유전자결핍(dMMR) 미발현 그룹에서 ORR 38.3%(CR:10.6%)을 기록했다.
- [동정]유한양행, 23년 연속 존경받는 기업 제약부문 1위 수상
- [인사]티씨노바이오사이언스, 정진아 신임 개발본부장(CDO) 영입
- [부음]한원선 前 한원선신경정신과의원 원장 별세
- [동정]인천성모병원 이운정교수, 응급의료 공로로 소방청장 표창
- [동정]충남대병원 박재호 물리치료사, 연구논문 국제학술지 게재
- [동정]경희대병원 여승근 교수, 대한민국의학한림원 정회원 선출
- [동정]건양대병원 차아름 씨, 외국인 환자 유치 유공 대전시장 표창
- [동정]세종충남대병원 박재형・오진경 교수, 대한내과학회 수여 ‘KJIM 최다인용 공로상’ 선정
- [동정]범석학술장학재단, 제29회 범석상에 김병극·김승현 교수 선정
- [부음]김권식 메디포뉴스 전무 빙모상
- [인사]티씨노바이오사이언스, 정진아 신임 개발본부장(CDO) 영입
- [인사]서울성모병원 장기육 교수, 대한심혈관중재학회 차기 회장 추대
- [인사]영남대 영천병원, 제18대 박삼국 병원장 취임
- [인사]명지병원, ‘뇌졸중 전문가’ 최영빈 교수 영입
- [인사]동산의료원·동산병원·대구동산병원 보직인사(2/1)
- [인사]삼성서울병원, 원장단 및 주요 보직 인사(2/1)
- [인사]배재훈 교수, 계명대학교 동산의료원장 취임
- [인사]동화약품, 장재원 연구개발본부장 선임
- [인사]HLB 자회사 엘레바, 김동건 대표 선임
- [인사]서울대병원 우홍균 교수, 아시아방사선종양학회연합회 회장 취임
- [동정]유한양행, 23년 연속 존경받는 기업 제약부문 1위 수상
- [동정]인천성모병원 이운정교수, 응급의료 공로로 소방청장 표창
- [동정]충남대병원 박재호 물리치료사, 연구논문 국제학술지 게재
- [동정]경희대병원 여승근 교수, 대한민국의학한림원 정회원 선출
- [동정]건양대병원 차아름 씨, 외국인 환자 유치 유공 대전시장 표창
- [동정]세종충남대병원 박재형・오진경 교수, 대한내과학회 수여 ‘KJIM 최다인용 공로상’ 선정
- [동정]범석학술장학재단, 제29회 범석상에 김병극·김승현 교수 선정
- [동정]인천성모병원 이순규 교수, 대한간암학회 학술대회 우수구연상 수상
- [동정]명지병원 김민석 교수, 제62차 세계흉부외과학회 ‘Maxwell Chamberlain 논문상’
- [동정]고대 구로병원 병리과, 서울특별시장 표창·서울시의회 의장상 동시 수상













