하이, 범불안장애 디지털 의료기기 임상시험 결과 탑 저널 게재
임상 효과는 치료 종료 후 5주까지 지속 확인
- 노영희 기자 nyh2152@medifonews.com
- 등록 2025-10-20 10:04:33
디지털 헬스케어 기업 하이(대표이사 김진우)는 정서장애 디지털 의료기기로는 최초로 식약처 품목허가를 획득한 엥자이랙스(Anzeilax)의 임상 시험 결과가 관련 분야 탑 저널 중 하나인 JMIR (Journal of Medical Internet Research) 본지 10월 판에 게재됐다고 밝혔다.
하이의 논문 ‘Efficacy of a Smartphone-Based Digital Therapeutic (Anzeilax) in Generalized Anxiety Disorder: Randomized Controlled Trial’이 글로벌 탑 저널인 JMIR에 게재됐다. 본 논문에서 진행된 임상시험은 강남세브란스 병원에서 2023년 8월에서 2024년 8월까지 총 13개월간 진행되었다.
임상시험 총 참여자는 96명으로 실험군과 대조군에 각 48명씩 배정됐다. 임상 진행은 TAU (Treatment As Usual) 방식으로 진행되었으며 실험군 참여자는 복용하는 약과 더불어 엥자이랙스를 사용했고 대조군은 약만 복용하는 방식으로 진행됐다. 임상시험 기간은 총 10주간 진행했고 후속 관찰을 위해 15주 시점에서도 평가를 시행했다.
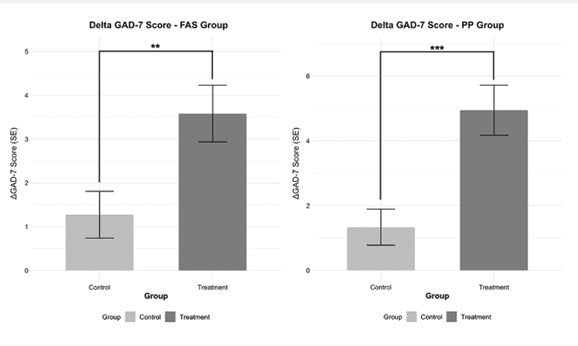
주 평가 지표는 GAD(Generalized Anxiety Disorder)-7 점수 변화였고, 보조 평가 지표로 BAI (Beck Anxiety Inventory), PSWQ (Penn State Worry Questionnaire), HADS-A / HADS-D (Hospital Anxiety and Depression Scale-불안/우울 부분) 등이 포함됐다.
임상군의 GAD-7 초기 점수는 실험군이 12.4, 대조군이 12.3점으로 거의 차이가 없었다. 그러나 임상 시험 종료 결과는 상당한 차이가 있는 것으로 나타났다. 먼저 약만 복용한 대조군의 10주 후 GAD-7 점수는 11.04로 약 11% 개선된 반면, 엥자이랙스를 함께 사용한 실험군의 GAD-7점수는 29% 개선된 8.83점으로 약 3배 정도 효과가 높은 것으로 나타났다. 또한, 이런 결과는 추적 관찰 시점(15주)에서도 효과가 유지되는 것으로 나타났다.
본 논문은 JMIR Publications 홈페이지에서 확인할 수 있다.
하이 김진우 대표는 “본 임상 시험결과가 국제적으로 인정받아 기쁘게 생각한다. 본 결과에 의하면, 엥자이랙스가 현재 중증 불안장애로 많은 어려움을 겪고 있는 분들에게 충분히 고려할 만한 좋은 대안이 될 수 있을 것이다”고 본 논문 게재의 의의를 밝혔다.
하이는 소비자가 엥자이랙스를 처방받고 사용할 수 있도록 판매와 관련해 마무리 작업을 진행 중이다. 실제 병원에서 처방을 받아 사용할 수 있는 시기는 2025년 11월에서 12월 사이가 예상된다고 밝혔다. 소비자들이 소프트웨어 형태의 디지털 치료기기를 접하는 것이 익숙하지 않은 만큼, 회사는 사용자들의 편의를 위해, 다양한 지원 방안을 준비 중이며, 정서장애 디지털 치료기기 처방에 관심이 있는 병원을 모집 중에 있다고 밝혔다.
관련기사
- 하이, 2025 전국사회복지관대회 ‘스마트 헬스체크 이벤트’ 진행 2025-05-22
- 하이, BIO KOREA서 비침습 혈당측정 가능한 ‘글루코첵’ 전시 2025-05-07
- 하이, 범불안장애 DTX ‘엥자이렉스’ 품목허가 획득 2025-04-09
- 하이, 언어장애 재활 개선 앱 개시 미팅 진행 2025-02-24
- 하이, CES 2025에서 AI 활용 디지털 헬스케어 진단 서비스 호평 2025-01-09
- 하이-수원과대, 디지털 헬스케어 활성화 위한 전략적 업무협약 체결 2024-11-04
- 하이, 디지털 의료기기 확산 참여 공공기관 모집 (~9/27) 2024-09-10
- 하이-티에이치케이컴퍼니와 업무 제휴로 디지털 헬스케어 사업확대 2024-09-06
- 하이, 인지기능 평가 및 맞춤형 개선 서비스 ‘새미랑’ 조달청 혁신제품 선정 2024-09-02
- 하이, 마비말장애 재활 디지털치료제 리피치 美 MGH ‘임상연구’ 승인 획득 2024-08-26
- 하이, 아이엠재활병원과 포괄적 업무협약 체결 2024-06-18
- 하이, 치매 진단 디지털 의료기기 알츠가드 식약처 확증적 임상 승인 획득 2024-04-25
- 하이, 마비말장애 재활 DTx ‘리피치’ 식약처 확증적 임상 승인 획득 2024-02-26
- 하이, 美 MGH 보건전문대학원과 확증적 임상 수행 계약 체결 2023-12-13
- 디지털 헬스케어의 비즈니스 모델, 앞서간 기업에게 듣다 2023-12-12
- 하이, LG생활건강 임직원에 ‘마음정원’ 서비스 제공 2023-11-15
- 하이, 신임 이사회 의장에 신희영 전 대한적십자사 총재 선임 2023-10-04
- 디지털치료제 기업 하이, 2022년 마음건강 트렌드 보고서 발간 2023-02-23
- 하이-증평노인복지관, AI 활용 경도인지장애 선별 업무협약 체결 2023-01-06
- [동정]박지만 서울치대 교수, 과학기술진흥유공 부총리표창 수상
- [부음]강원경 가톨릭대 여의도성모병원장 모친상
- [동정]부산대병원, 대한정형외과학회 유튜브 콘텐츠 경진대회 대상 수상
- [동정]길병원 방제호 교수, 'PAAFPRS & KAFPRS 2026' 국제학회 최우수 구연상 수상
- [인사]고대 구로병원 나승운 교수, ‘대한임상노인학회 이사장’ 취임
- [동정]제약바이오협회 홍보전문위원장에 문종훈 종근당 이사
- [동정]전남대병원 비뇨의학과, 국내 주요 학술대회서 연이은 수상
- [동정]강동경희대학교병원 차재명 교수, '서울 국제 소화기질환 심포지엄' 공로상 수상
- [동정]동국제약 인사돌, ‘2026 국가산업대상’ 잇몸약 부문 대상 수상
- [동정]건양대병원 김용석 의료정보원장, 국무총리 표창 수상
- [인사]고대 구로병원 나승운 교수, ‘대한임상노인학회 이사장’ 취임
- [인사]범부처재생의료기술개발사업, 박장환 2대 사업단장 선임
- [인사]식약처 고위공무원 인사 (4/15)
- [인사]길병원 박기형 교수, 대한치매학회 이사장 취임
- [인사]휴온스바이오파마, 이정희 신임 대표 선임
- [인사]중앙대병원 이정규 교수, 대한성형안과학회 회장 취임
- [인사]동화약품, 신용재 중선파마 호치민 지사장 선임
- [인사]건강보험심사평가원 홍승권 신임 원장 임명
- [인사]고대 안산병원 신승용 교수, 순환기의공학회 이사장 취임
- [인사]순천향대 부천병원 문종호 교수, ‘제19대 대한췌장담도학회 이사장’ 취임
- [동정]박지만 서울치대 교수, 과학기술진흥유공 부총리표창 수상
- [동정]부산대병원, 대한정형외과학회 유튜브 콘텐츠 경진대회 대상 수상
- [동정]길병원 방제호 교수, 'PAAFPRS & KAFPRS 2026' 국제학회 최우수 구연상 수상
- [동정]제약바이오협회 홍보전문위원장에 문종훈 종근당 이사
- [동정]전남대병원 비뇨의학과, 국내 주요 학술대회서 연이은 수상
- [동정]강동경희대학교병원 차재명 교수, '서울 국제 소화기질환 심포지엄' 공로상 수상
- [동정]동국제약 인사돌, ‘2026 국가산업대상’ 잇몸약 부문 대상 수상
- [동정]건양대병원 김용석 의료정보원장, 국무총리 표창 수상
- [동정]일산백병원 이태승 교수, 대한소화기학회 ‘우수 구연상’ 수상
- [동정]제7회 ‘임세원 추모 의학상’에 고려대학교 구로병원 이문수 교수
- [화촉]김영천 신신제약 전무(영업본부장) 딸 (4/19)
- [화촉]김학경 지오영 병원영업본부 부사장 아들 (4/19)
- [화촉]이승구 이화의료원 홍보전략팀 사무원(3/21)
- [화촉]경남지오영 노순섭 부사장 딸 (12/27)
- [화촉]박진규 대한신경외과병원협의회 회장 딸 (12/14)
- [화촉]장규열 한림제약 사장 아들 (11/29)
- [화촉]배대길 종근당 홍보실장 딸 (11/9)
- [화촉]이애형 경기도약사회 대외협력본부장 아들 (10/18)
- [화촉]유재신 前 광주광역시약사회장 아들 (10/25)
- [화촉]오승주 前 현대약품 부사장 딸 (9/20)








