의약품허가, 구조적 변화 중…ETC 허가감소 추세
[5년 동향] 올 상반기 2612품목허가 전년동기 25% 감소
- 전유미 기자 yumi5596@medifonews.com
- 등록 2009-07-24 10:27:44
올 상반기 의약품 허가(신고) 품목은 총 2612품목으로 전년동기 3464품목이 허가된 것에 비해 24.6% 감소한 것으로 나타났다.
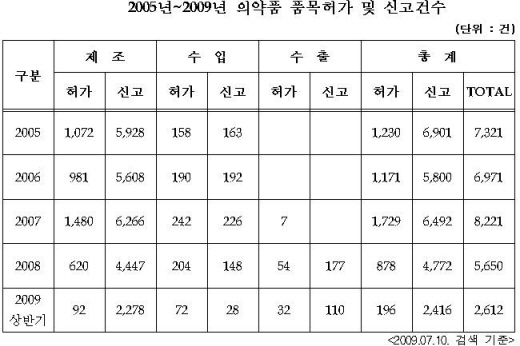
24일 식약청이 발표한 2009년 상반기 의약품 허가현황에 따르면, 2004년부터 5개년간의 허가(신고) 현황을 비교한 결과 2008년부터 품목허가(신고) 건수가 전년도에 비해 감소하는 경향이 나타났으며, 특히 2009년 상반기는 전문의약품 허가(신고)의 감소 경향이 두드러졌다.
이와관련해 식약청은 2008년 7월 1일부터 전문의약품에 있어 품목별 사전 GMP평가가 의무화됨에 따라 철저한 품질관리가 가능한 품목만이 허가받을 수 있게됨으로써 발생한 결과로 풀이했다.
또한, 2009년 상반기까지 총 허가(신고)된 품목은 원료의약품 및 한약재를 제외하고, 전문의약품 24,303품목, 일반의약품 18,210품목으로 총 42,513품목으로 집계됐다.
약효별 1위“자양강장 관련 제품”, 수출 경쟁력 항생제 우위
식약청은 약효군별로는 2009년 상반기 허가(신고) 품목수는 질환의 치료에 사용되는 의약품보다는 ‘혼합비타민제’, ‘단백아미노산제’ 및 ‘칼슘제’ 등 자양강장 관련제품의 허가가 272 품목으로, 총 허가 건수의 22%를 차지했다고 발표했다.
이는 인구고령화와 경제성장으로 건강에 대한 사회적인 관심이 고조되면서 이른바 해피 드럭(Happy Drug)에 대한 소비자들의 수요가 크게 증가하고 있음을 보여준다.
이와함께 항생제의 경우 허가(신고)된 52개 품목 중 46개 품목인 88%가 수출용으로 허가됐다. 반면 항암제의 경우 허가(신고)된 7개 품목 중 5개 품목이 수입품목으로 항생제와 대조적인 양상을 보였다.
생동성입증 총 5821품목, 2009년상반기 리센트론산나트륨 57품목 추가
2001년 이후 현재까지 생물학적동등성 공고 품목은 총 5,821 품목으로 이 중 생물학적동등성 시험을 실시한 품목은 총 5,073 품목이며, 나머지는 비교용출시험 또는 이화학적동등성시험을 실시했다. 다만, 약물의 특성상 비교임상시험을 통해 공고된 제품도 1품목 있었다.
또한 2009년 상반기 공고된 273개 품목 중 허가받은 회사에서 직접 생산하는 품목은 135품목, 생산을 위탁하는 품목은 138품목으로 집계됐다.
참고로, 제네릭 의약품의 경우 독성에 관한 자료, 약리작용에 관한 자료 및 임상시험성적에 대한 자료를 제출하는 대신 생물학적동등성시험자료로 허가받을 수 있다.
DMF 완료 총 907품목, 한국 및 인도의 원료가 50% 차지
식약청은 DMF 검토를 완료한 원료의약품은 현재까지 총 907품목, 2009년 상반기에 추가된 품목은 신물질 원료의약품 21개를 포함해 총 58개로 나타났다.
이중 한국에서 생산하는 원료가 302개, 인도가 155개, 일본 및 중국이 각각 58개, 56개를 차지하고 있는것으로 드러났다.
식약청 관계자는 “현재 DMF 대상은 2002년 7월1일 이후 허가된 신약의 유효성분인 신물질 원료의약품, 다빈도 사용 등이 인정되어 고시된 원료 등이며, 장기적으로는 선진국과 같이 완제의약품에 사용되는 모든 유효성분을 대상으로 DMF를 추진할 계획이다”고 밝혔다.
참고로, DMF(원료의약품신고) 제도는 원료의약품을 관리하는 제도로써 부정.불량 원료의 사용을 차단하여 의약품의 품질을 확보하기 위하여 2002년 7월부터 도입된 제도이다.
한편, 2009년 상반기동안 원료의약품은 총 209품목이 허가됐으며, 이 중 43%는 국내에서 제조하고, 57%는 생산이 완료된 제품을 수입하여 국내에서 포장하는 ‘소분’제조 품목으로 나타났다.
하지만, 소분제조 품목의 주 생산국은 중국으로, 향후 중국의 의약품 제조 및 품질 관리정책 및 동향 등에 대한 철저한 모니터링이 요구되고 있다.
- [동정]병협 첫 여성회장 탄생…유경하 이대의료원장 당선
- [동정]제주대학교병원 강현식·박경기 교수, 암예방 공로로 보건복지부장관 표창
- [동정]영남대병원 허민구 교수, 대한안과학회 '율산학술상' 수상
- [동정]건양대병원 김하영 전공의, 국제췌담도학회 ‘우수 구연상’
- [동정]고대 안암병원 이형래 교수, 대한정형외과 스포츠의학회 춘계학술대회 우수구연상 수상
- [동정]인천성모병원 이정훈 교수, ‘대한유방갑상선외과의사회 우수연제상’ 수상
- [인사]동화약품, 신용재 중선파마 호치민 지사장 선임
- [인사]건강보험심사평가원 홍승권 신임 원장 임명
- [동정]서울대병원 박중신 교수, 제54회 보건의 날 ‘황조근정훈장’ 수훈
- [동정]이대목동병원 유선아 전임의, 소화기기능성질환·운동학회 ‘젊은 연구자상’ 수상
- [인사]동화약품, 신용재 중선파마 호치민 지사장 선임
- [인사]건강보험심사평가원 홍승권 신임 원장 임명
- [인사]고대 안산병원 신승용 교수, 순환기의공학회 이사장 취임
- [인사]순천향대 부천병원 문종호 교수, ‘제19대 대한췌장담도학회 이사장’ 취임
- [인사]SK바이오, R&D 실행력 강화 위해 연구지원조직 정비 및 핵심인재 영입
- [인사]화순전남대병원 김인영 교수, 대한정위기능신경외과학회장 선임
- [인사]원광대병원 김정우 교수, 대한견주관절학회 제34대 회장 취임
- [인사]일동제약그룹 정기승진인사 (4/1)
- [인사]한국산텐제약, 신임 대표이사에 김진희 대표 선임 (4/1)
- [인사]일동제약, 새 R&D 본부장 박재홍 사장 선임
- [동정]병협 첫 여성회장 탄생…유경하 이대의료원장 당선
- [동정]제주대학교병원 강현식·박경기 교수, 암예방 공로로 보건복지부장관 표창
- [동정]영남대병원 허민구 교수, 대한안과학회 '율산학술상' 수상
- [동정]건양대병원 김하영 전공의, 국제췌담도학회 ‘우수 구연상’
- [동정]고대 안암병원 이형래 교수, 대한정형외과 스포츠의학회 춘계학술대회 우수구연상 수상
- [동정]인천성모병원 이정훈 교수, ‘대한유방갑상선외과의사회 우수연제상’ 수상
- [동정]서울대병원 박중신 교수, 제54회 보건의 날 ‘황조근정훈장’ 수훈
- [동정]이대목동병원 유선아 전임의, 소화기기능성질환·운동학회 ‘젊은 연구자상’ 수상
- [동정]가정의학과의사회 유승호 공보이사, 보건복지부 장관상 수상
- [동정]경북대병원 김혜정 연구교수·박준석 교수 연구팀, 대한대장항문학회 ‘우수포스터상’ 수상








