국내 임상 질·양적 ‘상종가’…상반기 202건 증가
지역 기관별 편중현상 지속-서울·경기, 빅5병원 독주
- 임설화 기자 shlim@medifonews.com
- 등록 2010-07-28 10:12:29
경제 불황으로 전세계 전체임상 건수는 감소하고 있는 반면 국내 임상은 질적 양적으로 성장하고 있다.
28일 식품의약품안전청(청장 노연홍)에 따르면 2010년 상반기까지 승인된 202건의 임상시험을 분석한 결과 국내 임상의 꾸준한 성장세가 눈에 띈다.
국내 임상산업의 국제경쟁력의 지표가 될 수 있는 초기 임상시험(0~1상)이 전체 임상시험에서 차지하는 비율은 ‘08년 87건(21.8%)에서 ’09년 85건(21.3%), ‘10년 6월 현재 55건(27.2%)으로 상승 분위기다.
이는 국내 임상시험기관의 의료 전문 인력과 시설 등 인프라 및 임상시험의 질적 수준이 점차적으로 국제적 경쟁력을 갖추고 있는 데 따른 것으로 분석된다.
전세계 임상건수는 ‘07년 1만2278건에서 ‘08년 1만5388건, ’09년 1만5252건으로 감소했으나 국내 식약청 승인 임상 건수는 ‘09년 상반기 169건에서 ‘10년 상반기 202건으로 증가했다.
올상반기 승인된 임상시험 중 다국적 제약사의 임상시험은 95건으로 전체 건수(202건) 중 절반 정도를 차지하는 것으로 나타났다.
임상시험 신청 의뢰자는 2008년부터 2010년 상반기까지 한국화이자제약(53건, 5.3%), 글락소스미스클라인(42건, 4.2%), 한국노바티스(39건, 3.9%), 한국얀센(36건, 3.6%), 퀸타일즈트랜스내셔널코리아(31건, 3.1%) 순으로 상위 5개사가 모두 다국적 제약사였다.
이어 서울대학교병원(30건, 3.0%)과 서울아산병원(29건, 2.9%) 등 시험기관이 6위와 7위를 차지해 연구자 임상시험도 활발히 수행되고 있는 것으로 나타났으며, 국내 제약사 중에서는 한미약품(29건, 2.8%)이 유일하게 상위 10위권내 포함됐다.
하지만 올상반기에도 임상시험 수행의 지역별, 기관별 편중현상은 여전히 계속됐다.
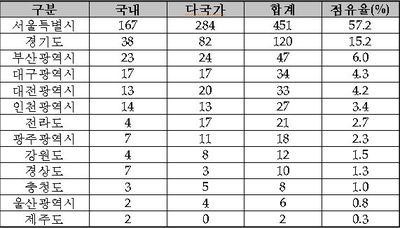
임상시험 수행 지역별로는 서울(57.2%) 및 경기도(15.2%)에서 대부분의 임상시험이 실시되는 것으로 조사됐다.
임상시험 기관별로는 2008년부터 2010년 상반기까지 총 142개 기관(‘10년 6월말 현재) 중 서울대학교병원(355건, 35.4%), 서울아산병원(343건, 34.2%), 연세대학교신촌세브란스병원(340건, 33.9%), 삼성서울병원(339건, 33.8%), 가톨릭대학교서울성모병원(184건, 18.4%) 등 이른바 빅5 기관이 활동이 여전히 강세다.
특히 올 상반기 신약개발 초기 임상시험(0·1상)은 서울대학교병원(14건, 25.5%), 서울아산병원(11건, 20%), 삼성서울병원(11건, 20%), 연세대학교신촌세브란스병원(10건, 18.1%), 고려대학교안암병원(9건, 16.4%) 등 순으로 0·1상 수행기관 전체 69건(병원건수) 중 55건을 빅5 기관이 점유했다.
이는 0·1상이 고도의 기술과 인프라를 갖춘 기관만이 수행할 수 있는 데 따른 것으로 풀이된다.
2008년부터 2010년 상반기까지 임상시험 치료영역별로는 종양(259건, 25.9%), 심혈관계(138건, 13.8%), 정신신경계(115건, 11.5%) 의약품의 임상시험이 같은 기간 전체 임상시험의 절반 가량을 차지했다.
식약청은 이같은 임상시험 편중현상 해소하기 위해 글로벌 임상국가 도약을 위한 임상시험 경쟁력 강화방안을 마련해 추진중이다.
주요 강화방안으로는 ▲의약품 및 의료기기 임상시험 실시기관 지정 절차 간소화 ▲의약품·의료기기 임상시험 관련 제도·규정의 조화 ▲임상시험심사위원회(IRB) 운영 통합관리 ▲의약품임상시험용 의료기기 통관절차 개선 등이다.
또한 초기 임상시험 경쟁력을 높이기 위해 ▲승인처리기간을 14일로 단축 ▲상담기간 단축 및 절차 간소화 등 사전상담제 개선 ▲자가점검요약서 도입 ▲그간 한글번역에 따른 시간적 경제적 부담이었던 영문계획서 제출 허용 등을 추진하고 있다.
아울러 국제적 수준의 임상시험 안전관리 방안으로 ▲임상시험 전자자료 관리 규정 및 가이드라인 제정 ▲임상시험심사위원회(IRB)의 안전성 보고의무 강화 ▲임상시험 실시상황보고에 대한 국제적 기준(ICH-E2F) 도입 등을 계획하고 있다.
한편 임상시험계획 승인 소요기간(공휴일, 보완기간은 제외)은 2008년 평균 35.5일, 2009년 28.6일, 2010년 상반기 28.1일로 단축됐으며, 올상반기 연구자 주도 임상시험 승인기간은 20.6일로 2009년 25.5일에 비해 가장 크게 줄었다.
- [동정]고대 안산병원 박종학 교수, 보건복지부장관 표창
- [동정]길병원 박상현 교수팀, 대한피부과학회 ‘최우수 구연상’ 수상
- [동정]고대 안암병원 이성우 교수, 대한정위기능신경외과학회 최우수 포스터상 수상
- [인사]리가켐바이오 김용주 대표, 회장으로 승진
- [인사]신임 부산대학교병원장에 김해영 교수 임명
- [부음]공병훈 연세아너스치과의원 원장 장인상
- [동정]국민건강보험 일산병원 송민주 교수, 美 근관치료학회 학술지 논문상 수상
- [인사]한국신약개발연구조합, 국제협력 자문위원 2인 위촉
- [동정]길병원 이태훈 의료원장, ‘국민훈장 동백장’ 수훈
- [동정]멀츠 에스테틱스, ‘글로벌 지속가능 브랜드∙리더 100’ 2년 연속 선정
- [인사]리가켐바이오 김용주 대표, 회장으로 승진
- [인사]신임 부산대학교병원장에 김해영 교수 임명
- [인사]한국신약개발연구조합, 국제협력 자문위원 2인 위촉
- [인사]고대 구로병원 나승운 교수, ‘대한임상노인학회 이사장’ 취임
- [인사]범부처재생의료기술개발사업, 박장환 2대 사업단장 선임
- [인사]식약처 고위공무원 인사 (4/15)
- [인사]길병원 박기형 교수, 대한치매학회 이사장 취임
- [인사]휴온스바이오파마, 이정희 신임 대표 선임
- [인사]중앙대병원 이정규 교수, 대한성형안과학회 회장 취임
- [인사]동화약품, 신용재 중선파마 호치민 지사장 선임
- [동정]고대 안산병원 박종학 교수, 보건복지부장관 표창
- [동정]길병원 박상현 교수팀, 대한피부과학회 ‘최우수 구연상’ 수상
- [동정]고대 안암병원 이성우 교수, 대한정위기능신경외과학회 최우수 포스터상 수상
- [동정]국민건강보험 일산병원 송민주 교수, 美 근관치료학회 학술지 논문상 수상
- [동정]길병원 이태훈 의료원장, ‘국민훈장 동백장’ 수훈
- [동정]멀츠 에스테틱스, ‘글로벌 지속가능 브랜드∙리더 100’ 2년 연속 선정
- [동정]중앙대광명병원 김혜리 교수, 대한신경정신의학회 춘계학술대회 우수포스터상 수상
- [동정]박지만 서울치대 교수, 과학기술진흥유공 부총리표창 수상
- [동정]부산대병원, 대한정형외과학회 유튜브 콘텐츠 경진대회 대상 수상
- [동정]길병원 방제호 교수, 'PAAFPRS & KAFPRS 2026' 국제학회 최우수 구연상 수상
- [화촉]김영천 신신제약 전무(영업본부장) 딸 (4/19)
- [화촉]김학경 지오영 병원영업본부 부사장 아들 (4/19)
- [화촉]이승구 이화의료원 홍보전략팀 사무원(3/21)
- [화촉]경남지오영 노순섭 부사장 딸 (12/27)
- [화촉]박진규 대한신경외과병원협의회 회장 딸 (12/14)
- [화촉]장규열 한림제약 사장 아들 (11/29)
- [화촉]배대길 종근당 홍보실장 딸 (11/9)
- [화촉]이애형 경기도약사회 대외협력본부장 아들 (10/18)
- [화촉]유재신 前 광주광역시약사회장 아들 (10/25)
- [화촉]오승주 前 현대약품 부사장 딸 (9/20)













